
考试说明要求
考试内容 | 要求 |
1.通过化学键的断裂与形成,能说明化学反应中能量转化的原因 2.通过化学能与热能、化学能与电能的相互转化,认识常见的能量转化形式及其重要应用 3.能正确书写热化学方程式并根据盖斯定律进行有关计算 | Ⅰ Ⅰ Ⅱ |
解读:化学反应与能量是中学化学教学的核心内容之一,是与生产生活实际密切相关的内容,体现着化学学科的社会价值,属于新课程教材新增内容,在新课程高考中属于热点内容之一,化学能与热能相互转化的主要题型为:
①书写热化学方程式、②通过化学键键能计算反应热、③通过图像信息计算反应热、④应用盖斯定律的有关计算。这块知识在学习时一定要依据本质建构各种角度的认知模型,依据模型解题,并在解题时需要细心,准确计算,注意化学用语表达的规范性。
最近又出现反应热与能源结合起来进行考查。由于能源问题已成为社会热点,有关能源的试题也将成为今后命题的重点。《考试说明》化学反应与能量增加了,了解燃烧热和中和热等概念;这要引起足够的重视。预计考查反应热的内容将不断拓宽,难度有所提高,题型也会有新的变化。能量及其转化是化学、物理、生物学科中的一个重要内容,是理科综合试题的知识载体之一,因此有关能量的学科间的综合将会成为今后理科综合命题的热点。
知识清单
一.化学反应中的能量变化
1、化学反应中的能量变化,通常表现为热量的变化:
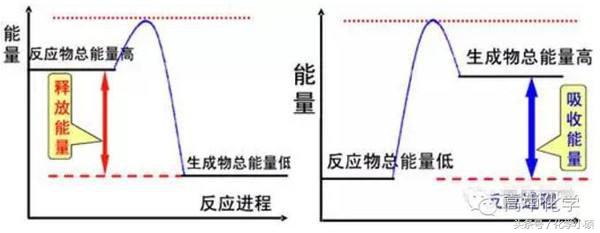
①吸热反应:化学上把吸收热量的化学反应称为吸热反应。
②放热反应:化学上把放出热量的化学反应称为放热反应。
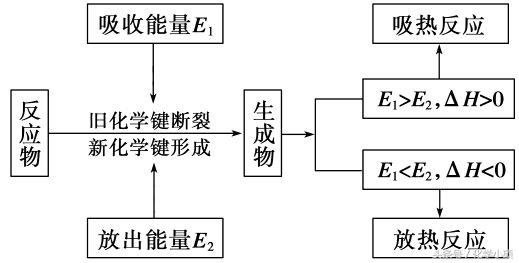
2、化学反应中能量变化的本质原因
化学反应中的能量变化与反应物和生成物所具有的总能量有关。如果反应物所具有的总能量高于生成物所具有的总能量,在发生化学反应时放出热量;如果反应物所具有的总能量低于生成物所具有的总能量,在发生化学反应时吸收热量。
3、反应热、燃烧热、中和热
①反应热:在化学反应中放出或吸收的热量,通常叫反应热用△H表示。单位:kJ·mol–1
②燃烧热:在101kPa时1mol 物质完全燃烧生成稳定的氧化物时所放出的能量,叫该物质的燃烧热。如:101kPa时lmol H2完全燃烧生成液态水,放出285.5 kJ·mol–1的热量,这就是H2的燃烧热。 H2(g)+12 O2 (g) =H2O(l);△H=–285.5kJ·mol–1
③中和热:在稀溶液中,酸和碱发生中和反应而生成1mol H2O,这时的反应热叫做中和热。
H+(aq)+OH–(aq)=H2O(1);△H=–57.3kJ·mol–1(强酸和强碱的中和热)
二、热化学方程式
1、定义:表明反应所放出或吸收的热量的方程式,叫做热化学方程式。
2、热化学方程式书写注意事项:
(1).△H只能写在标有反应物和生成物状态的化学方程式的右边,并用“;”隔开。若
为放热反应,△H为“-”;若为吸热反应,△H为“+”。△H的单位一般为kJ/mol。
(2).注意反应热△H与测定条件(温度.压强等)有关。因此书写热化学方程式时应注
明△H的测定条件绝大多数△H是在25℃.101325Pa下测定的,可不注明温度和压强。
(3).注意热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,
并不表示物质的分子 或原子数。因此化学计量数可以是整数.也可以是分数。
(4).注意反应物和产物的聚集状态不同,反应热△H不同。因此,必须注明物质的聚
集状态才能完整地体现出热化学方程式的意义。气体用“g”,液体用“l”,固体用“s”,溶液
用“aq”。热化学方程式中不用↑和↓
(5).注意热化学方程式是表示反应已完成的数量。由于△H与反应完成物质的量有关,所以方程式中化学式前面的化学计量数必须与△H相对应,如果化学计量数加倍,则△H也要加倍。
(6)当反应逆向进行时,反应热数值相等,符号相反;两个热化学方程式相加或相减,可得到新的热化学方程式。
三.盖斯定律
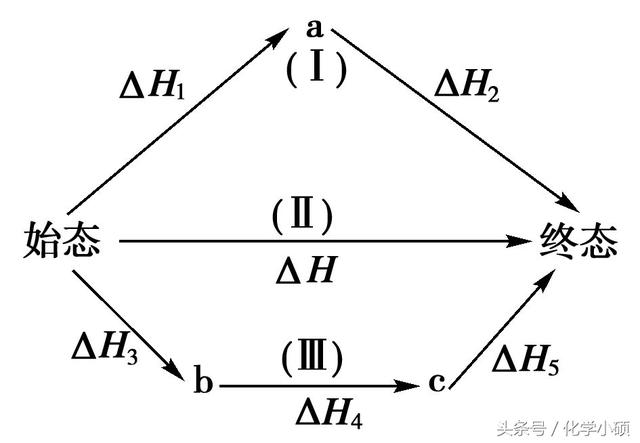
①一般计算的方法是:将ΔH看作热化学方程式中的一项,再按有关化学方程式的计算步骤、格式进行计算,得出有关数据。
②盖斯定律的应用:如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的。
 加载中,请稍侯......
加载中,请稍侯......
精彩评论