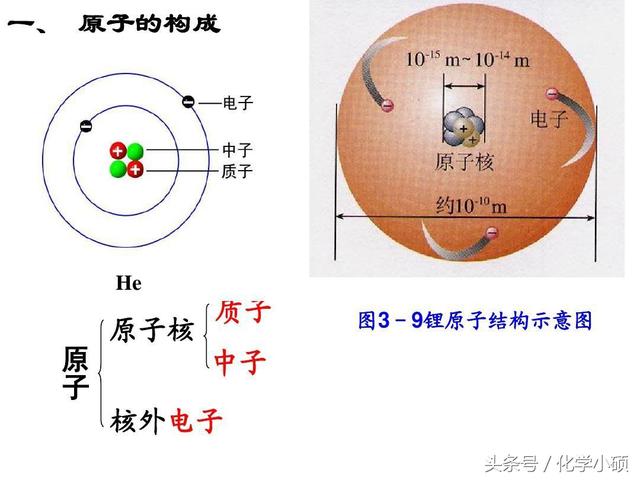
考点1 原子结构
【例1】美国科学家将两种元素铅和氢的原子核对撞,获得了一种质子数为118,中子数为175的超重元素,该元素原子核内的中子数与核外电子数之差是( ) ’
A 57 B 47 C 61 D.293
【思路分析】对原子而言,核外电子数等于质子数,故中子数与核外电子数之差为:175—118=57。
【答案】A 。
1—1.(拓展题)美国科学家分析海水沉积
物时发现,北大西洋和太平洋海水中的14360Nd和14460Nd(元素钕)的含量差异明显,由此得出周围大陆的岩石中14360Nd和14460Nd含量不同的结论。下列有关说法正确的是( )
A 14360Nd和14460Nd互为同素异形体
B 元素Nd是主族元素
C 14360Nd和14460Nd中质量数和中子数均不相同
D.因各地岩石中14360Nd和14460Nd含量不同,所以Nd元素没有固定的相对原子质量
1—2.(易错题)美国铱星公司(已破产)原计划发射77颗卫星,以实现全球卫星通讯,其要发射卫星的数目恰好与铱元素的原子核外电子数目相等。下列关于铱元素的各种说法中正确的是( )
A铱原子的质子数为70
B铱原子的相对原子质量为77
C铱原子的质子数为77
D.铱元素为非金属元素
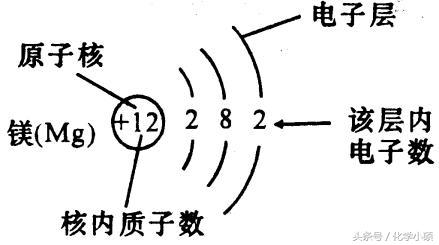
考点2 元素、核素与同位素
【例2】(2005年广东高考)Se是人体必需微量元素。下列关于7834Se和8034Se的说法正确的是( )
A 7834Se和8034Se互为同素异形体
B 7834Se和8034Se为同位素
C 7834Se和8034Se分别含有44个和46个质子
D 7834Se和8034Se都含有34个中子
【思路分析7834Se和8034Se具有相同棱电荷数,且属同类原子,故互为同位素;7834Se和8034Se都含34个质子,中子数分别为44、46。
【答案】B ‘, ·
2—1.(拓展题)据报道,用10B合成的10B20有非常好的抗癌作用。下列叙述正确的是( )
A 10B和10B20互为同位素
B 10B和10B20互为同素异形体
C 10B的中子数和核外电子数不相等
D 10B20表示由20个10B原子形成的一种硼分子
2—2.(易错题)下列各组物质中,互为同位素的是( )
A石墨和金刚石 H水和重水(D20)
C纯碱和烧碱 D.氕和氘
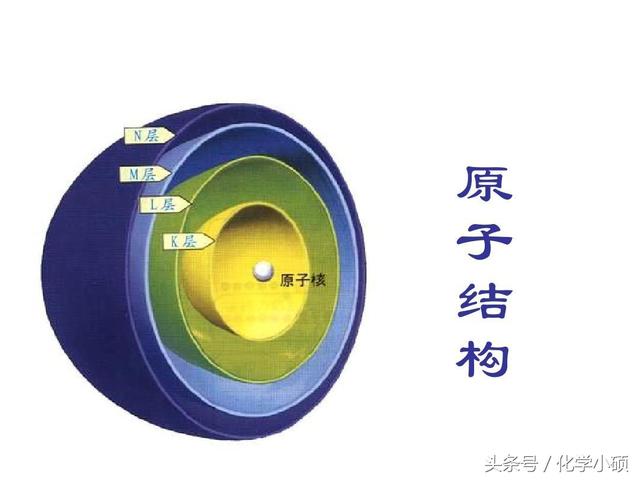
考点3 原子核外电子排布规律
【例3】在第n电子层中,当它作为原子的最外层时,容纳数最多与(n一1)层相同。当它作为电子的次外层时,其电子I(n+1)层最多能多10个,则此电子层是( )
A K层 B L层
C M层 D-N层 j
【思路分析】由题意很容易排除A、B两项。M层作为最I最多容纳8个,与L层相同;而当M层作为次外层最多填18比L层多10个。
【答案】C i
3--1.(拓展题)下列各原子构成的单质中,肯定能与稀硫酸应产生H2的是( )
A 原子核内没有中子
B M层有5个电子 }
C 原子核外最外层电子数=电子层数
D.N层上电子数与K层电子数相等,次外层有8个电子
3—2.(易错题)下列微粒结构示意图表示正确的是( )
考点4 相对原子质量 、
【例4】160中的“16”表示的含义是( )
A 氧元素的相对原子质量
B 氧元素的一种同位素的近似相对原子质量
C 氧元素的近似相对原子质量
D.氧元素的一种同位素的质量数
【思路分析】元素的相对原子质量是该元素的各种同位素的相质子质量(Ar)与其丰度(%)乘积的和的值,故A错误;同位素的对原子质量是该同位素一个原子的绝对质量与12C质量的1/12的比值。同位素的近似相对原子质量是该同位素一个原子的质量与12C质量的1/12的比值的近似整数倍,在数值上与同的质量数相等。因此,BD正确。元素的近似相对原子质量同位素的近似相对原子质量(即质量数)与其丰度乘积的和
C错误。
答案:BD 、
I 4-1.(拓展题)硼有两种天然同位素12B和11B,已知硼元素的量为10.8。下列对硼元素中12B的质量分数的判断正确的是
A 等于20% B 小于20%
C 略大于20% D.等于80%
4-2.(易错题)某元素R的氧化物用R205表示。已知用15
15克与8克氧气完全反应生成R205,则R的原质量为( )
A 14 B 23 C 31 D 75

考点5 简单微粒半径的变化规律
【例5】下列化合物中阴离子半径和阳离子半径之比最大的是( )
A LiI B NaBr C.KCl D.CsF
【思路分析】离子的电子层数越多,半径越大,卤族离子中,I-的电子层最多,故半径最大,而碱金属中,Li+半径最小。
【答案】A
5—1.(易错题)关于同一种元素的原子或离子,下列叙述正确的是( )
A原子半径比阴离子半径小
B原子半径比阴离子半径大
C原子半径比阳离子半径小
D.带正电荷多的阳离子半径比带正电荷少的阳离子半径大
 加载中,请稍侯......
加载中,请稍侯......
精彩评论