初中化学溶液的浓度
基础知识梳理

5.氯化钠溶液的质量分数为16%,“16%”的意义:每100份质量的氯化钠溶液中含16份质量的氯化钠。
二、配制一定溶质质量分数的溶液
1.用固体配制溶液
仪器:__天平、药匙、量筒、胶头滴管、烧杯、玻璃棒__。
步骤:计算、称量、溶解、装瓶贴标签。
2.用浓溶液稀释
仪器:量筒、胶头滴管、烧杯、玻璃棒。
步骤:计算、量取、稀释、装瓶贴标签。
标签一般包括药品的名称(化学式)和浓度。
3.溶液的稀释计算
稀释的方法:加入溶剂或加入低浓度溶液。
关系式:
(1)加水稀释:__浓溶液质量×浓溶液溶质质量分数=稀释后溶液质量×稀释后溶液质量分数或浓溶液质量×浓溶液溶质质量分数=(浓溶液质量+加入水的质量)×稀释后溶液质量分数__。
(2)加入低浓度溶液稀释:__浓溶液质量×浓溶液溶质质量分数+稀溶液质量×稀溶液溶质质量分数=(浓溶液质量+稀溶液质量)×混合后所得溶液溶质的质量分数__。
注:①如果用固体配制溶液时,固体带有结晶水(例如硫酸铜晶体),那么所得溶液的溶质质量分数会偏小。
②量取液体时,如果仰视读数,量取的液体会偏多;如果俯视读数,量取的液体会偏少。
③用固体配制溶液时,天平未调平、砝码颠倒等情况会影响溶液的溶质质量分数。
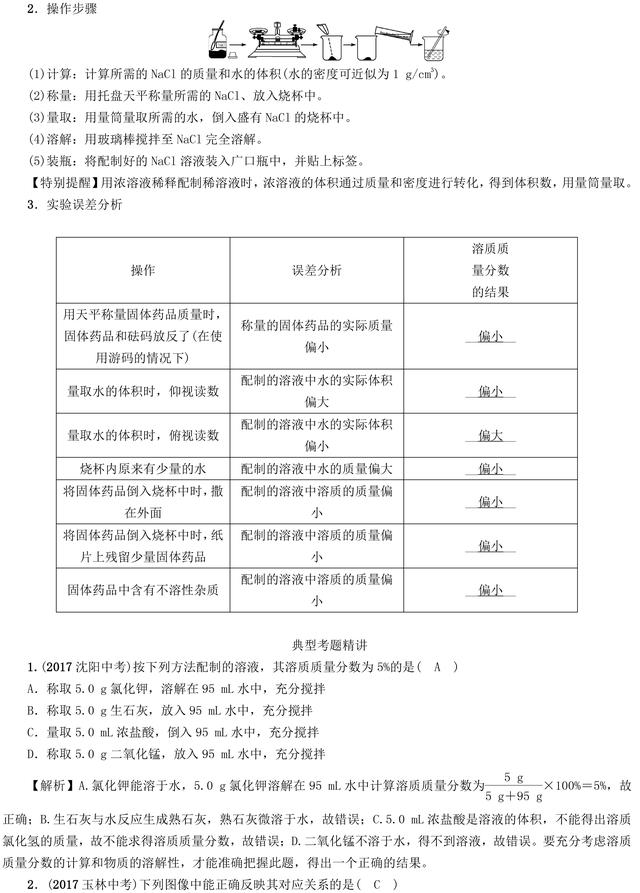
三、实验突破:一定溶质质量分数的氯化钠溶液的配制
1.实验仪器的选用及仪器的作用
(1)实验仪器:托盘天平(砝码和镊子)、药匙、胶头滴管、量筒、烧杯、玻璃棒。
(2)主要仪器作用:托盘天平:称量固体NaCl的质量。
【特别提醒】①在实验过程中,天平不能用来称量液体药品的质量;②称量时两只托盘垫上相同质量的纸片;③有腐蚀性(或易受潮)的药品应放在小烧杯或玻璃器皿中称量。
量筒:量取液体的体积,选用的量筒的量程比所量液体体积略大,且越接近越好。
玻璃棒:用来搅拌液体,加快固体溶质(或液体溶质)的溶解速率。


 加载中,请稍侯......
加载中,请稍侯......
精彩评论