




8、甲、乙两种固体的溶解度曲线如图所示。
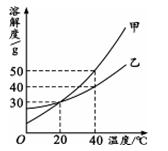
(1)______ ℃时,甲和乙的溶解度相等;
(2)40℃时,若将40g乙放入160g水中充分溶解,所得溶液的溶质质量分数为______ ,该溶液是______ 溶液(填“饱和”或“不饱和”);
(3)欲将40℃时乙物质的饱和溶液变为不饱和溶液,可采用的方法是______ ;
(4) 40℃时,将甲、乙两物质的饱和溶液各100g,分别降温到20℃,所得甲物质溶液的质量______(选填“>”或“=”或“<”)乙物质溶液的质量。
(5)将40℃时甲、乙两种物质的饱和溶液降温至20℃(其它条件不变),溶质的质量分数保持不变的是______
(6) 40℃时,将甲、乙两物质的饱和溶液各100g降温至20℃,析出晶体(均不含结晶水)的质量关系是:m(甲) ______ m(乙) (填“﹥”、“﹦”或“﹤”)。
(7)40℃,把50克的甲和20克的乙全部放入100克的水中,充分溶解后将溶液降温到20℃时,析出的固体及其质量是,由此得出从甲和乙的混合溶液中提纯甲的方法是______.
9、根据表中的数据,回答下列问题。
温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
溶解度 | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 |
(1)30℃时氯化钠的溶解度是__________,该温度下_________(填“能”或“不能”) 配制出45.8%的硝酸钾溶液。
(2)20℃时,称取31.6g KNO3固体加入盛有100g水的烧杯中,充分溶解形成的溶液是______(填“饱和”或“不饱和”)溶液;所得溶液的质量是 ;称取31.6g KNO3固体时,发现托盘天平指针偏右,接下来的操作是______。
(3)当KNO3中混有少量NaCl时,提纯KNO3所采用的方法是。
(4)当等质量KNO3的饱和溶液和NaCl的饱和溶液从60℃降温到20℃,对所得溶液的叙述正确的是(填序号)。
A.都是饱和溶液 B.溶剂质量:KNO3>NaCl C.溶液质量:KNO3<NaCl
(5)若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是(填序号)
A.0℃~20℃ B. 20℃~40℃ C. 40℃~60℃ D. 60℃~80℃
(6)70℃时,分别用100克水配制硝酸钾、氯化钠的饱和溶液,然后降温至20℃下列说法的是_________。
A、20℃时,得到的均为饱和溶液
B、析出的硝酸钾晶体比氯化钠晶体多
C、20℃时,硝酸钾溶液的浓度大于氯化钠溶液的浓度
(7)欲将一接近饱和的硝酸钾溶液转化为相同质量分数的饱和溶液,可采用的方法是___
 加载中,请稍侯......
加载中,请稍侯......
精彩评论