高中化学解题方法技巧之——守恒法
守恒法是高考中常考常用的一种解题方法。系统学习守恒法的应用,对提高解题速率和破解高考难题都有很大的帮助。
●难点磁场
请试做下列题目,然后自我界定学习本篇是否需要。
现有19.7g由Fe、FeO、Al、Al2O3组成的混合物,将它完全溶解在540mL 2.00 mol·L-1的H2SO4溶液中,收集到标准状况下的气体8.96L。已知混合物中,Fe、FeO、Al、Al2O3的质量分数分别为0.284、0.183、0.274和0.259。欲使溶液中的金属阳离子完全转化为氢氧化物沉淀,至少应加入2.70mol·L-1的NaOH(aq)体积是________。
●案例探究
[例题]将CaCl2和CaBr2的混合物13.400g溶于水配成500.00mL溶液,再通入过量的Cl2,完全反应后将溶液蒸干,得到干燥固体11.175g。则原配溶液中,c(Ca2+)∶c(Cl-)∶c(Br-)为
A.3∶2∶1 B.1∶2∶3 C.1∶3∶2 D.2∶3∶1
命题意图:考查学生对电荷守恒的认识。属化学教学中要求理解的内容。
知识依托:溶液等有关知识。
错解分析:误用电荷守恒:
n(Ca2+)=n(Cl-)+n(Br-),错选A。
解题思路:1个Ca2+所带电荷数为2,则根据溶液中阳离子所带正电荷总数等于阴离子所带负电荷总数,知原溶液中:
2n(Ca2+)= n (Cl-)+n (Br-)
将各备选项数值代入上式进行检验可知答案。
答案:D
●锦囊妙计
化学上,常用的守恒方法有以下几种:
1.电荷守恒
溶液中阳离子所带正电荷总数等于阴离子所带负电荷总数。即:阳离子物质的量(或浓度)与其所带电荷数乘积的代数和等于阴离子物质的量(或浓度)与其所带电荷数乘积的代数和。
2.电子守恒
化学反应中(或系列化学反应中)氧化剂所得电子总数等于还原剂所失电子总数。
3.原子守恒
系列反应中某原子(或原子团)个数(或物质的量)不变。以此为基础可求出与该原子(或原子团)相关连的某些物质的数量(如质量)。
4.质量守恒
包含两项内容:①质量守恒定律;②化学反应前后某原子(或原子团)的质量不变。
此外,还有物料平衡,将编排在第16篇——水的电离中。
1.(★★★)将3.48g Fe3O4完全溶解在100mL 1.00 mol/L的H24227(aq)25.00mL,恰好使Fe2+全部转化为Fe3+,且Cr272-全部转化为Cr3+27的物质的量浓度为。
2.(★★★)某露置的苛性钾经分析含水:7.62%(质量分数,下同)、K2CO3:2.38%、KOH:90.00%。取此样品1.00g放入46.00mL 1.00 mol·L-1的HCl(aq)中,过量的HCl可用1.070mol/L KOH(aq)中和至中性,蒸发中和后的溶液可得固体_______克。
3.(★★★★)A、B、C三种物质各15g,发生如下反应:
A+B+C--D
反应后生成D的质量为30g。然后在残留物中加入10g A,反应又继续进行,待反应再次停止,反应物中只剩余C,则下列说法正确的是
A.第一次反应停止时,剩余B9 g
B.第一次反应停止时,剩余C6 g
C.反应中A和C的质量比是5∶3
D.第二次反应后,C剩余5g
4.(★★★★★)
(1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO摩尔质量为74.7g·mol-1)。
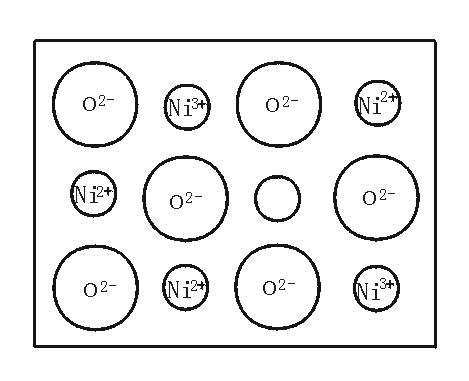
图1—1
(2)天然的和绝大部分人工制备的晶体,都存在各种缺陷,例如在某种NiO晶体中就存在如图1—1所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。
附:参考答案
难点磁场提示:根据Na原子守恒和SO4守恒得如下关系:1.提示:Fe3O4中+2价铁所失电子物质的量与Cr27中+6价铬所得电子物质的量相等。×(3-2)=0.02500 L×c(Cr2O72-)×(6-3)×2。
答案:0.100mol·L-1
2.提示:根据Cl原子守恒得:
n(KCl)= n(HCl)= 1.00 mol·L-1×0.04600L = 4.60×10-2mol,m(KCl)易求。
答案:3.43g
3.解析:第一次反应A不足,因为第一次反应后加入A又能进行第二次反应。第二次反应后,只剩余C,说明A、B恰好完全反应。则:
m反(A)∶m反(B)= (15 g+10g)∶15g = 5∶3
第一次反应耗B的质量mB为:15g∶mB=5∶3,mB=9g
即第一次反应后剩余B质量为:15g-9g=6 g。
可见(A)选项不正确。
根据mA+mB+mC=mD,可知生成30g D时消耗C的质量。
mC=30g-15g-9g=6 g
即第一次反应后剩余C质量为:15g-6g=9g。
又见(B)选项不正确。
易见反应消耗A、B、C质量之比为:mA∶mB∶mC=15g∶9g∶6g=5∶3∶2
(C)选项不正确。
答案:D
4.提示:由题得NiO晶体结构(如右图)。
其体积为:
V= (a×10-8cm)3
右图向三维空间延伸,它平均拥有的Ni2+、O2-数目为:
N(Ni2+)=N(O2-)=1/8×4==1/2N(NiO)
由密度公式得:
ρ(NiO)=
(2)(电荷守恒法)设1mol Ni0.97O中含Ni3+物质的量为x,则Ni2+的物质的量为(0.97mol-x);根据电荷守恒得:
3x+2×(0.97mol-x)=1mol×2 x=0.06mol
N(Ni3+)∶N(Ni2+)=0.06mol∶(0.97mol-0.06mol)=6∶91
答案:(1)
(2) 6∶91
 加载中,请稍侯......
加载中,请稍侯......
精彩评论