2021年新高考化学模拟练习题(文件编号:21022801)
目录:
2021年新高考化学模拟练习题01
2021年新高考化学模拟练习题02
2021年新高考化学模拟练习题03
2021年新高考化学模拟练习题04
2021年新高考化学模拟练习题05
关注微信公众号:cc518xxzl 可免费领取本资料word完整版!
简介:

可能用到的相对原子质量:H 1 C 12 N14 O 16 Fe 56
第一部分
本部分共 14 题,每题 3 分,共 42 分。在每题列出四个选项中,选出最符合题目要求
的一项。
1.我国科技创新成果斐然,下列成果与电化学无关的是 ( )
A | B | C | D |
|
|
|
|
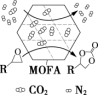
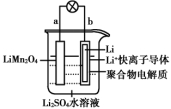
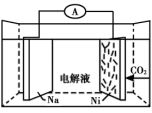
有机金属材料吸附与转化CO2 | 研发出水溶液锂 离子电池 | 研发出“可呼吸” Na—CO2电池 | 常温常压下用电解 法制备高纯H 2 |
答案:A
解析:A. 根据结构简式可知,双氢青蒿素的组成元素有C、H、O,属于有机物,A项正确;
B. 全氮阴离子盐中不含C元素,不属于有机物,B项错误;
C
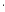
D. 砷化铌纳米带不含C元素,不属于有机物,D项错误;、答案选A。
2、(2019·浙江4月选考,10)下列说法正确的是( )
A.18O2和16O2互为同位素
B.正己烷和2,2-二甲基丙烷互为同系物
C.C60和C70是具有相同质子数的不同核素
D.H2NCH2COOCH3和CH3CH2NO2是同分异构体
答案 B
解析 18O2和16O2是相对分子质量不同的分子,而同位素指具有相同质子数,但中子数不同的元素,A项错误;正己烷的分子式为C6H14,2,2-二甲基丙烷即新戊烷分子式是C5H12,两者同属于烷烃,且分子式差一个CH2原子团,属于同系物,B项正确;核素表示具有一定的质子数和中子数的原子,C60和C70是由一定数目的碳原子形成的分子,显然,C项错误;H2NCH2COOCH3和CH3CH2NO2的分子式分别为C3H7O2N和C2H5O2N,分子式不同,显然不是同分异构体,D项错误。
3、下列说法中不正确的是
A.植物油氢化过程中发生了加成反应
B.苯和甲苯都能发生取代反应
C.氯乙烯和乙二醇都能用来作为合成高分子化合物的原料
D.变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
答案:D
解析:变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应;错误,是因为植物油被氧化成醛。发生的反应类型是氧化反应,所以D错误,选D。
4、设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
A.标准状况下,11.2L苯中含有C—H键的数目为3NA
B.常温下,1.0LpH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA
C.常温下,56g铁片投入足量浓硫酸中生成NA个SO2分子
D.电解饱和食盐水,阳极产生22.4L气体时,电路中通过的电子数目为2NA
答案 B
解析 标准状况下,苯不是气体,不能使用标准状况下的气体摩尔体积计算苯的物质的量,A项错误;常温下,pH=13的Ba(OH)2溶液中氢氧根离子浓度为0.1mol·L-1,1.0L该溶液中含有0.1mol氢氧根离子,含有的OH-数目为0.1NA,B项正确;常温下铁片与浓硫酸发生钝化现象,阻止了反应的继续进行,C项错误;因为温度、压强不明确,无法计算阳极生成22.4L气体的物质的量,D项错误。
5、某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。下列说法不正确的是( )
A.HAP能提高HCHO与O2的反应速率
B.HCHO在反应过程中,有C—H键发生断裂
C.根据图示信息,CO2分子中的氧原子全部来自O2
D.该反应可表示为:HCHO+O2HAPCO2+H2O
答案 C
解析 根据图知,HAP在第一步反应中作反应物、第二步反应中作生成物,所以为催化剂,催化剂能改变化学反应速率,故A项正确;HCHO在反应中有C—H键断裂和C===O键形成,所以甲醛被氧化生成二氧化碳和水,故B项正确;根据图知,CO2分子中的氧原子一部分还来自于甲醛,故C项错误;该反应中反应物是甲醛和氧气,生成物是二氧化碳和水,HAP为催化剂,反应方程式为HCHO+O2HAPCO2+H2O,故D项正确。
6、能正确表示下列反应的离子方程式为( )
A.向FeBr2溶液中通入过量Cl2:2Fe2++Cl2===2Fe3++2Cl-
B.向碳酸钠溶液中通入少量CO2:CO3+2CO2+H2O===2HCO3
C.向碘化钾溶液中加入少量双氧水:3H2O2+I-===IO3+3H2O
D.向硫化钠溶液中通入过量SO2:2S2-+5SO2+2H2O===3S↓+4HSO3
答案 D
解析 FeBr2电离产生的Fe2+、Br-都具有还原性,向该溶液中通入过量Cl2,阳离子、阴离子都会被氧化,离子方程式为:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-,A项错误;向碳酸钠溶液中通入少量CO2,Na2CO3、CO2、H2O发生反应产生NaHCO3,反应的离子方程式为:CO3+CO2+H2O===2HCO3,B项错误;H2O2具有氧化性,在酸性条件下,会将I-氧化为I2,反应的离子方程式为:H2O2+2H++2I-===I2+2H2O,C项错误;向硫化钠溶液中通入过量SO2,由于酸性:H2SO3>H2S,会发生S2-+SO2+H2O===H2S+SO3,SO2+2H2S===3S↓+2H2O,SO3+SO2+H2O===2HSO3,总反应方程式为2S2-+5SO2+2H2O===3S↓+4HSO3,D项正确。
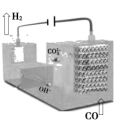
7、化学在生活中有着广泛的应用,下列反应关系正确的是( )
选项 | 化学性质 | 实际应用 |
A | FeCl3溶液显酸性 | 脱除燃气中的H2S |
B | Na2S溶液显碱性 | 去除废水中的Cu2+、Hg2+等 |
C | 活性炭具有还原性 | 用作自来水的净化剂 |
D | NaClO2具有氧化性 | 脱除烟气中的SO2及NOx |
答案 D
解析 脱除H2S利用FeCl3的氧化性,A项错误;去除废水中的Cu2+、Hg2+是利用S2-与Cu2+、Hg2+等形成沉淀,与Na2S溶液显弱碱性无关,B项错误;净化自来水是利用活性炭的吸附性,C项错误;NaClO2具有氧化性,将SO2及NOx转化为硫酸和硝酸而除去,D项正确。
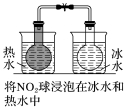
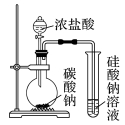
8、下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)( )
A | B | C | D | |
定律或原理 | 勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏加德罗定律 |
实验方案 |
|
|
|
|
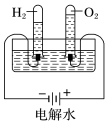
结果 | 左球气体颜色加深,右球气体颜色变浅 | 烧瓶中冒气泡,试管中出现浑浊 | 测得ΔH为ΔH1、ΔH2的和 | H2与O2的体积比约为2∶1 |
答案 B
解析 2NO2

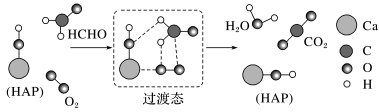
9、.含碳、氢、氧、氮四种元素的某医药中间体的3D模型如图甲所示。下列有关该物质的说法正确的是
A. 能发生取代反应,但不能发生加成反应
B. 可以与强碱反应,也能与强酸反应
C. 属于芳香族化合物,且与苯丙氨酸互为同系物
D. 其结构简式可表示为图乙,所有原子可能共面
答案B
解析:A. 由有机物的结构可知,存在碳碳双键,能发生加成反应,存在羧基,能发生取代反应,A项错误;
B. 有机物结构中存在羧基,能体现酸性,可与强碱反应,存在氨基,能体现碱性,因此也可与强酸反应,B项正确;
C. 有机物的结构中不存在苯环,不属于芳香族化合物,C项错误;
D. 乙为甲的结构简式,分子中六元环中含有2个亚甲基,具有四面体结构,因此所有原子不可能共面,D项错误;
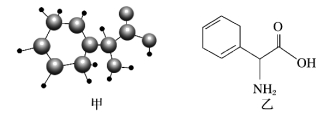
10.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。下列说法错误的是( )
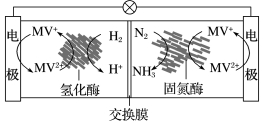
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应H2+2MV2+===2H++2MV+
C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D.电池工作时质子通过交换膜由负极区向正极区移动
答案 B
解析 由题图和题意知,电池总反应是3H2+N2===2NH3。该合成氨反应在常温下进行,并形成原电池产生电能,反应不需要高温、高压和催化剂,A项正确;观察题图知,左边电极发生氧化反应MV+-e-===MV2+,为负极,不是阴极,B项错误;正极区N2在固氮酶作用下发生还原反应生成NH3,C项正确;电池工作时,H+通过交换膜,由左侧(负极区)向右侧(正极区)迁移,D项正确。
11、BeCl2是有机反应的催化剂。铍和氯气反应的能量变化如图所示。下列说法正确的是( )
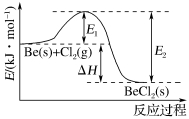
A.E2是正反应的活化能
B.该反应的ΔH<0
C.加入催化剂,ΔH减小
D.ΔH=E2-E1
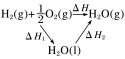
 加载中,请稍侯......
加载中,请稍侯......
精彩评论