粤教版九年级化学下册期中专项复习:基本概念(文件编号:21022522)
关注微信公众号:cc518xxzl 可免费领取本资料word完整版!
简介:
粤教版九年级化学下册期中专项复习:基本概念
基本概念
【学习目标】
1.理解基本概念的含义,初步学会运用概念解决实际问题。
2.学会常用化学用语的书写并理解其含义。
3.学会运用元素化合物知识解决问题。
【重点】对基础知识的理解
【难点】运用基础知识解决问题
【自主探究】
1.物理变化与化学变化两者之间本质区别是 .
2.实验室用红磷燃烧来测定空气成分, 集气瓶中,观察到的现象是 。反应停止,等集气瓶冷却后,打开弹簧夹,烧杯中的水会 大约达到集气瓶体积的 为止。此实验说明集气瓶中有 ,大约![]() 占 体积,剩余 体积主要是 气。上述实验中往往产生误差较大,你认为可能的原因是 .
占 体积,剩余 体积主要是 气。上述实验中往往产生误差较大,你认为可能的原因是 .
3.燃烧必须具备的条件是: , , 。
4.分子是保持物质 的一种微粒;原子是 中的最小微粒;二者的本质区别是 ;
5.原子是由居于原子中心的带 的 和核外带 电的 构成的,而原子核又可以再分,它是由 和 两种微粒构成的。在原子中, 数、 数、 数三者相等;
6.元素与元素的本质区别是 ;元素符号表示的意义 、 ;化学式CO2表示的含义是 、 、
、 。
2N表示 ;3H2O表示 ;2Mg2+表示 。
7.净化水常用的方法有 、 、 ;其中净化程度最高的是 ;硬水与软水鉴别方法 ,有浮渣产生或泡沫较少的是 ,泡沫较多的是 。
8.质量守恒定律的内容是_____________的各物质的质量_______等于_______的各物质
质量_____,这个规律叫做质量守恒定律。化学反应前后,肯定没有发生变化的是________ ,肯定发生变化的是 ,可变可不变的是 。化学反应的实质是:反应物的_______破裂成_______,_______重新组合![]() 成_______ 。
成_______ 。
9.概括氢气的物理性质:通常状况下,氢气是___色____味___体,密度比空气________ ,______于水。氢气不同于气体气体最显著的特征是 。氢气可以燃烧,火焰为 色,有 生成,会有 放出。点燃氢气须 。
10.碳单质有 、 、活性炭、C60等。金刚石和石墨的物理性质有很多差异的原因是 。木炭和活性炭都具有 性,利用这个性质,活性炭可做防毒面具的滤![]() 毒剂。
毒剂。
11.碳单质的化学性质
(1)常温下碳的化学性质很 。
(2)碳的可燃性:a充分燃烧的化学方程式 为 ;不充分燃烧的化学方程式为 。
(3)在高温条件下,炽热的碳可和二氧化碳反应生成 ,该反应的化学方程式为 。
12.通常情况下,一氧化碳是 、 的气体, 溶于水,密度比空 气 。具有 性。
13. 二氧化碳的物理性质标准状况下,二氧化碳是一种 、 、密度比空气 、 溶于水的气体。在一定条件下,二氧化碳能变成固体,俗称“ ”,它易 。
14. 二氧化碳的化学性质:(1)一般情况下二![]() 氧化碳不 也不 。
氧化碳不 也不 。
(2)CO2通入水中生成 ,反应的化学方程式为 ![]() ,碳酸不稳定,易分解,反应的化学方程式 。(3)向澄清石灰水里通入CO2,石灰水变 ,这是由于生成了 的缘故,其化学方程式为 ,利用这个反应可鉴定CO2气体。
,碳酸不稳定,易分解,反应的化学方程式 。(3)向澄清石灰水里通入CO2,石灰水变 ,这是由于生成了 的缘故,其化学方程式为 ,利用这个反应可鉴定CO2气体。
15.金属的化学性质有(1) (2) (3) ;金属活动性顺序表 。
【合作探究】
1.下列是日常生活![]() 中常发生的一些变化,其中都属于化学变化的一组是 ( )
中常发生的一些变化,其中都属于化学变化的一组是 ( )
A . 水受热沸腾,酒精燃烧 B. 汽油挥发,铁铸成锅
C. 食物腐烂,动植物呼吸 D. 瓷碗破碎,钢铁生锈
2. 下列元素符号既能表示一种元素,也能表示一个原子,还能表示一种物质的是 ( )
A.O B.N![]() C .Cu D .H
C .Cu D .H
3.下列各组物质中,前者是单质,后者是氧化物的是 ( )
A.石灰石 冰 B.金刚石 干冰 C.液氧 高锰酸钾 D.水银 碘酒
4.下列关于分子和原子的说法中,不正确的是 ( )
A.分子、原子都在不停地运动 ![]() B.分子、原子都是构成物质的微粒
B.分子、原子都是构成物质的微粒
C.原子是不能再分的最小微粒 D.分子是保持物质化学性质的最小微粒![]()
5.有下列说法,①呼吸作用、食物腐烂、铁生锈都是缓慢氧化反应②通常讲的燃烧是可燃物与空气中的氧气发生的剧烈氧化反应 ③急速燃烧一定会发生爆炸 ④自燃在空气中和在氧气中着火点不同 ⑤自燃是缓慢氧化引起的 ⑥燃烧、自燃、缓慢氧化的共同点都是氧化反应并且都放出热量,其中正确的是 ( )
A①②③ B.①④⑤ C.③④⑤ D.①②⑤⑥
6.在化学反应前后,下列各项①原子数目;②分子数目;③元素种类;④物质的总质量;⑤物质种类;⑥原子种类。肯定没有发生变化的是 ( )
A.①③④⑤⑥ B.①③④⑥![]() C.①④⑥ D.①③⑤
C.①④⑥ D.①③⑤
7.x、y、z三种金属中,只有z能和稀硫酸反应,当把y放入x的盐溶液中,y表面有x析出,则x、y、z三种金属的活动性顺序为 ( )
A.x>z>y B.y>x>z C.z>y>x D.y>z>x
8.自然界中几乎不存在纯净的水,若要对自然界中的水净化处理,其中净化程度最高的是
( )
A.吸附 B.沉淀 C.过滤 D.蒸馏
9.下列用途既利用了物质的物理性质,又利用了化学性质的是 ( )
A.用CO2灭火 B.用干冰人工降雨
C. 用CO2制作碳酸饮料 D.温室中用CO2做气体肥料
10.铟元素的核电荷数为49,相![]() 对原子质量为115,则铟原子核外电子数 ,中子数为 。
对原子质量为115,则铟原子核外电子数 ,中子数为 。
11.用化学符号表示:
2个氮原子 2个氮分子 2个铁离子 2个亚铁离子
2个铁原子 n个水分子 1个铵根离子 2个氢氧根离子
12. 下列物质①铜丝 ②二氧化碳 ③液氧 ④高锰酸钾 ⑤澄清石灰水 ⑥铁水 ⑦水银 ⑧冰水共存物⑨空气 ⑩氯化钠,其中属于混![]() 合物的是 ;属于化合物的是
合物的是 ;属于化合物的是
氧化物有 , 单质有 。
13.溶解度曲线为我们定量描述物质的溶解性强弱提供了便利。请你根据右图的溶解度曲线回答下列问题:
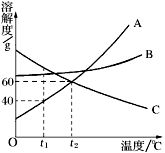 (1) t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 ;
(1) t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 ;
(2) 当A中混有少量B时,可用 ![]() 方法提纯A;
方法提纯A;
(3) 在t1℃时,将25 g A物质加入到盛有50 g水的烧杯中,充分搅拌,再升温至t2℃(不考虑溶剂的挥发),在升温过程中,A溶液中溶质的质量分数的变化情况是 。
 加载中,请稍侯......
加载中,请稍侯......
精彩评论