氧化还原反应方程式的配平
氧化还原反应的实质是反应过程中发生了电子转移,而氧化剂得电子的总数(或元素化合价降低总数)必然等于还原剂失电子总数(或元素化合价升高总数),根据这一原则可以对氧化还原反应的化学方程式进行配平。
配平过程一定要遵循一下两个守恒
电子守恒:在一个氧化还原反应中氧化剂得电子总数等于还原剂失电子总数。
化合价守恒:有关元素化合价升高总数等于另一些有关元素化合价降低总数。
配平的步骤:

配平方法
(1)全变从左边配:氧化剂、还原剂中某元素化合价全变的,一般从左边反应物着手配平。
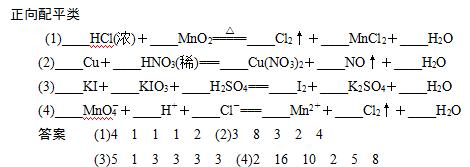
(2)自变从右边配:自身氧化还原反应(包括分解、歧化)一般从右边着手配平。
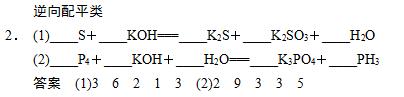
(3)缺项配平法:先使得失电子数配平,再观察两边电荷。若反应物这边缺正电荷,一般加(H+),生成物一边加水;若反应物这边缺负电荷,一般加(OH-),生成物一边加水。然后进行两边电荷数配平。
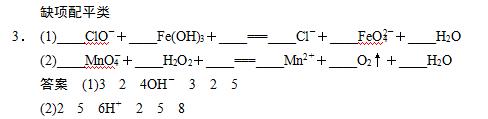
 加载中,请稍侯......
加载中,请稍侯......
精彩评论