考题训练(五)__空气与氧气
夯 实 基 础
1.【2017·郴州】空气是一种成分复杂的混合物,其中约占空气体积 21%的气体是( )
A.N2 B.CO2
C.稀有气体 D.O2
2.【2017·南京】下列行为会增加空气中 PM2.5 的是( )
A.治理工地扬尘 B.露天焚烧垃圾
C.使用公共自行车 D.禁止焚烧秸秆
3.【2017·潍坊】如图 K5-1是空气成分体积分数柱状示意图。其中"a"代表的是( )
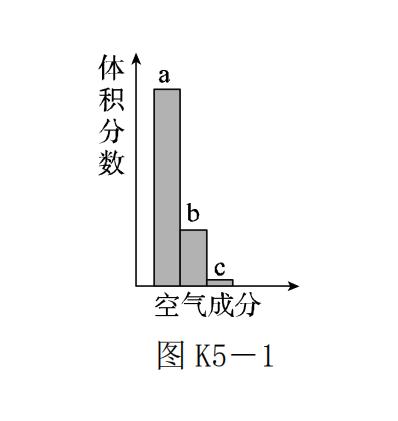
A.氮气
B.氧气
C.二氧化碳
D.稀有气体
4.【2017·广州】下列物质属于氧化物的是( )
A.O2 B.SiO2
C.Cu2(OH)2CO3 D.Fe(OH)3
5.【2017·天津】下列有关催化剂的说法正确的是( )
A.在化学反应后其质量减少
B.催化剂能改变化学反应速率
C.在化学反应后其质量增加
D.在化学反应后其化学性质发生了变化
6.【2017·邵阳】下列有关物质燃烧实验现象的描述正确的是( )
A.红磷在空气中燃烧,产生大量白烟
B.硫在空气中燃烧,发出明亮的蓝紫色火焰
C.木炭在氧气中燃烧,发出白光,生成二氧化碳
D.铁在空气中剧烈燃烧,火星四射,生成黑色固体
7.【2017·菏泽】如图 K5-2 是用红磷燃烧法测定空气中氧气含量的装置,有关此实验的结论与分析错误的是
( )
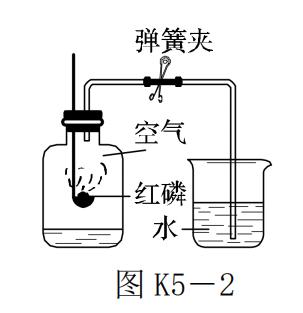
A.此实验证明,氧气约占空气体积的1
5
B.此实验证明,反应后集气瓶内剩余的气体,既不易溶于水,也不支持燃烧
C.该实验中的红磷还可以用硫来代替
D.若该实验没有达到预期目的,可能的原因之一是装置的气密性不好
8.【2016·淄博】下表是根据一些反应事实或现象推理得出的影响化学反应的主要因素,其中不合理的是( )
选项 化学反应事实(或现象) 影响因素
A过氧化氢在常温下分解速率比较慢,加入二氧化锰后迅
速分解催化剂
B 食物在冰箱中保存不易变质 温度
C蜡烛在空气中燃烧发出黄色火焰,在纯氧中燃烧火焰明
亮
反应物的
种类
D细铁丝在空气中不能燃烧,在纯氧中剧烈燃烧,火星四
射
反应物的
浓度
9.【2017·呼和浩特】如图 K5-3是实验室制取气体的几种发生装置和收集装置。请回答下列问题。
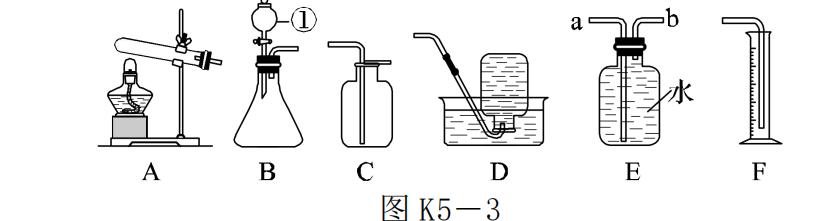
(1)写出标号①的仪器名称:____________。
(2)实验室用过氧化氢溶液和二氧化锰制取并收集较纯净的氧气时,应选用的装置是________(填字母),写出
该反应的化学方程式:______________________________________。
(3)将图中 E 和 F 装置连接,可以测量氧气的体积,氧气应从________(填"a"或"b")口通入。
10.PM2.5 是指大气中直径小于或等于 2.5 μm 的颗粒物,主要来自化石燃料的燃烧和扬尘,对人体健康和空
气质量的影响很大。
(1)计入空气污染指数的项目中除了可吸入颗粒物外,还包括________(填序号,下同)。
A.CO B.CO2 C.SO2 D.NO2
(2)下列关于 PM2.5 的说法错误的是________。
A.燃放烟花爆竹会产生 PM2.5
B.PM2.5 是造成雾霾天气的"元凶"之一
C.PM2.5 的颗粒大小与分子大小差不多
D.PM2.5 专用口罩使用了活性炭,是利用了活性炭的吸附性
能 力 提 升
1.【2017·齐齐哈尔】请答题的同学深呼吸,平静一下情绪。刚才吸入的空气中含量最多的气体是( )
A.氧气 B.稀有气体
C.氮气 D.二氧化碳
2.【2017·呼和浩特】空气是人类宝贵的自然资源。下列有关说法不正确的是( )
A.氧气可用作火箭发射的燃料
B.空气可用于工业制备氮气和氧气
C.氦气可用来填充探空气球
D.二氧化碳是植物进行光合作用的基本原料
3.【2017·广州】下列关于氧气的说法不正确的是( )
A.O2可以支持燃烧
B.O2可用排水法收集
C.O2可用于医疗急救
D.细铁丝在 O2中燃烧生成 Fe2O3
4.【2017·苏州】下列关于氧气的说法中,不正确的是( )
A.氧气能支持燃烧,所以氧气可作燃料
B.氧气能使带火星的木条复燃
C.红磷在氧气中燃烧,产生大量的白烟
D.实验室加热高锰酸钾制取氧气时,试管内靠近导管处放一团蓬松的棉花
5.【2017·长沙】请根据图 K5-4中提供的信息,回答问题。
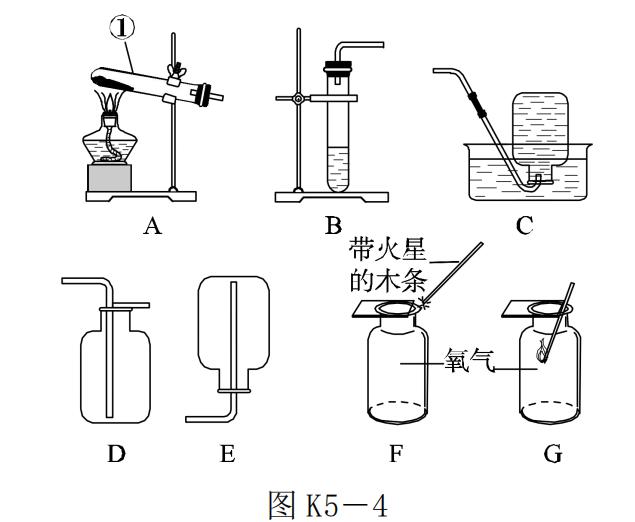
(1)写出装置图 A 中标号①的仪器名称:______。
(2)实验室用加热氯酸钾和二氧化锰的方法制取氧气,应选用的发生装置为________(填字母)。
(3)检验氧气是否收集满的正确操作是________(填字母)。
6.【2017·台州】为探究催化剂对过氧化氢溶液(H2O2)分解的催化效果,某研究小组做了如下实验。
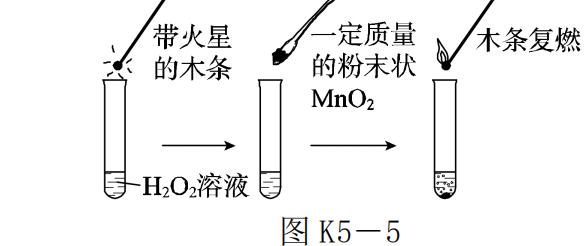
实验一:图 K5- 5 中的实验能否证明 MnO2 是过氧化氢溶液分解反应的催化剂,并说明理由:
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
图 K5-5
实验二:数据记录表
1% H2O2溶液/mL 50 50 50
加入 MnO2的质量/g 0.1 0.2 0.4
测量 40 s 末得到 O2体积/mL
从 表 格 的 设 计 可 以 看 出 , 该 实 验 的 目 的 是
________________________________________________________________________
________________________________________________________________________。
7.【2017·南京】空气中氧气含量测定的经典赏析。
教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图 K5-6 所示)。

资料卡片:
汞
密度:13.546 g/cm3
沸点:356.58 ℃
加热至沸时与氧气反应 氧化汞,密度:11.14 g/cm3,不能溶于汞,分解温度:500 ℃)
(1)写出汞与氧气反应的化学方程式:__________________________。
(2)本实验中选择使用汞的优点有:
①汞在加热的条件下,只和氧气反应。
②汞为液态,在汞槽中起到液封的作用,并能直接用来测量反应器内空间体积的变化。
③生成的氧化汞分解又能得到汞和氧气,把得到的氧气加到剩下的4
5体积的气体中,结果所得气体跟空气的性
质完全一样。
根据资料卡片,请再补充本实验使用汞的两个优点,并说明依据。
④________________________________________________________________________
________________________________________________________________________。
⑤________________________________________________________________________
________________________________________________________________________。
(3)通过实验,拉瓦锡得出了空气由氧气和氮气组成,其中氧气约占空气总体积1
5的结论。请根据现在的认识,
对此结论予以补充:________________________________________________________________________
________________________________________________________________________。
参考答案
|夯实基础|
1.D 2.B 3.A 4.B
5.B [解析] 催化剂能改变化学反应的速率,在反应前后化学性质和质量都不发生变化。
6.A [解析] 硫在空气中燃烧发出微弱的淡蓝色火焰,在氧气中燃烧发出明亮的蓝紫色火焰,都生成有刺激
性气味的气体;描述现象时不能说出产物的名称;铁在氧气中剧烈燃烧,火星四射,放出大量的热,生成黑色固体。
7.C [解析] 硫燃烧会生成二氧化硫气体,从而影响氧气体积的测定,所以不可以用硫来代替红磷。
8.C
9.(1)分液漏斗
(2)BD 2H2O2=====MnO2
2H2O+O2↑
(3)b
[解析] (1)由图知,仪器①为分液漏斗。(2)过氧化氢溶液与二氧化锰固体在常温下接触即可生成氧气,发生
装置应选择 B;由于氧气密度大于空气且不易溶于水,可采用排水法或向上排空气法收集,但排水法收集的氧气纯
度较高,所以收集装置应选 D,该反应的化学方程式为 2H2O2=====MnO2
2H2O+O2↑。(3)用 E 装置采用排水集气法收集氧气
时,氧气应由 b口通入,水从 a 口排出至量筒中,可测量收集氧气的体积。
10.(1)ACD (2)C
|能力提升|
1.C
2.A [解析] 氧气具有助燃性,但不具有可燃性,不能作燃料。
3.D [解析] 细铁丝在氧气中燃烧生成 Fe3O4而非 Fe2O3。
4.A
5.(1)试管 (2)A (3)F
[解析] (1)仪器①是试管,常用于加热少量的固体和液体或作少量物质反应的容器。(2)实验室用加热氯酸钾
和二氧化锰的方法制取氧气,反应物都是固体,反应需要加热,发生装置应选择 A。(3)验满气体的操作,应在集气
瓶口进行,正确的操作是 F。
6.实验一:不能证明,虽然能改变反应速率,但无法判断 MnO2在反应前后的质量和化学性质有无改变
实验二:探究二氧化锰的质量与化学反应速率的关系
7.(1)2Hg+O2=====△
2HgO
(2)④汞的沸点较低,汞蒸气与氧气反应比较充分,能将密闭装置内空气中的氧气几乎耗尽
⑤氧化汞的密度小于汞,且不溶于汞,因此易与汞分离(合理答案均可)
(3)空气的成分按体积计算大约是氧气 21%、氮气 78%、稀有气体等其他成分 1%
[解析] (1)汞与氧气在加热时反应,生成氧化汞,发生反应的化学方程式为 2Hg+O2=====△
2HgO。(2)从卡片信息
可知,本实验使用汞除题给三个优点外,还具有的优点是①汞的沸点较低,汞蒸气与氧气反应比较充分,能将密闭
装置内空气中的氧气几乎耗尽;②氧化汞的密度小于汞,且不溶于汞,因此易与汞分离。(3)拉瓦锡通过实验得出
空气是由氧气和氮气组成的结论,也大体得出空气中氧气约占其总体积的1
5。现代精确的实验证明,空气中氧气约
占其总体积的 21%、氮气约占 78%、稀有气体等其他成分约占 1%。

 加载中,请稍侯......
加载中,请稍侯......
精彩评论