题型训练(三)
[物质推断题]
1.某钠盐溶液中含有Cl-、OH-、CO32-三种阴离子。仅用一份样品溶液,利用下面的试剂与操作就可将溶液中的三种阴离子依次检验出来,正确的实验操作顺序是( )
①滴加Mg(NO3)2溶液 ②过滤③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③ C.③②①②④ D.④②③②①
2.一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种。为确定其组成,某同学设计了如下实验方案,下列判断正确的是( )
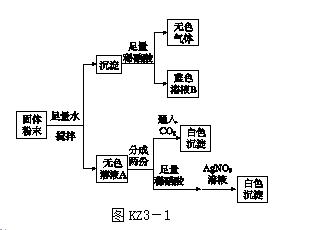
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
3.某固体可能含有Ca(NO3)2、Na2SO4、Na2CO3、FeCl3、KCl中的一种或几种,现对其进行如下实验:①取少量固体于试管中,加适量蒸馏水,固体完全溶解成无色透明溶液;②取少量上述溶液,加过量稀硫酸,有气泡产生;③取②所得溶液少量,滴加BaCl2溶液,产生白色沉淀。分析以上实验现象,下列对原固体组成的推断正确的是( )
A.肯定有Na2CO3、Na2SO4,无FeCl3、Ca(NO3)2
B.肯定有Na2CO3,无FeCl3、Ca(NO3)2
C.肯定有Na2CO3、Na2SO4,无FeCl3
D.肯定有Na2CO3,无FeCl3、KCl
4.下列四组物质,从左至右都能发生化学反应的是( )
(如:a与b能反应 b与c能反应 c与d能反应)
A.①②③ B.①③④ C.①③ D.①②③④
5.在下列转化关系中,各物质均是初中化学常见物质,其中甲、乙、丙属于单质,A为黑色固体,C属于盐。
回答下列问题。
(1)用化学式表示:乙________;B________。
(2)反应②的化学方程式为____________________________。
(3)反应④的化学方程式为____________________________________________。
6.现有甲、乙、丙、丁四种无色溶液,它们分别是稀盐酸、稀硫酸、BaCl2溶液、Na2CO3溶液中的一种,已知甲+乙→无明显现象,乙+丙→白色沉淀,丙+丁→白色沉淀,甲+丁→无色气体;BaCO3、BaSO4难溶于水。试回答:
(1)丁物质中的溶质是__________(填化学式)。
(2)写出乙和丙反应的化学方程式:____________________________________________。
(3)写出甲和丁反应的化学方程式:____________________________________________。
7.2016·菏泽A~G表示初中化学常见的物质,其中C是大理石的主要成分,各物质间相互转化的关系如图KZ3-2所示。请回答下列问题。
(1)B的化学式为________,反应④属于化学基本反应类型中的__________________。
(2)A是一种常见的钠盐,它的一种俗称是______________;反应③的化学方程式为________________________________。
8. A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,H为蓝色的硫酸盐溶液。它们的转化关系如图KZ3-3所示,回答下列问题。
(1)B的化学式为________,H中溶质的化学式为________。
(2)反应③的化学反应方程式为________________________。
(3)反应①~③中为置换反应的是__________(填序号)。
(4)写出稀盐酸与B反应的化学方程式:_________________________________。
9. A~K为中学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,他们之间的转换关系如图KZ3-4所示。
回答下列问题。
(1)写出D、F的化学式:D________;F________。
(2)①的基本反应类型为________________________________________________________________________。
(3)反应②的化学反应方程为____________________________________。
(4)气体E的用途是______________(写一条)。
10.如图KZ3-5所示,A是氧化物,可作干燥剂;D是一种盐,用于制造玻璃、洗涤剂等,它们之间发生如图变化,请你根据所学的化学知识作出推断。
(1)写出化学式:A________;D________。
(2)贝壳的主要成分是____________(写名称),贝壳高温煅烧的化学方程式为____________________________。
(3)Beq o(――→,s\up7(高温))F的化学方程式为__________________;E+H→蓝色沉淀的化学方程式是________________________。
(4)Geq o(――→,s\up7(AgNO3))H的基本反应类型是________反应。
(5)C的用途是__________________。
11. A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分。它们之间的部分转化关系如图KZ3-6所示(图中反应条件及部分反应物、生成物已省略)。
回答下列问题。
(1)写出下列物质的化学式:A______________;D______________。
(2)写出由物质C转化为物质B的化学方程式:____________________________。
(3)写出物质C与过氧化钠(Na2O2)反应生成碳酸钠和物质A的化学方程式:________________________________。
12. A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图KZ3-7所示的关系("→"表示物质经一步反应可转化为另一种物质,"—"表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)。
(1)若A、B为组成元素相同的气体,E为大理石的主要成分,则B的化学式为________;物质D的类别为________(填"酸""碱""盐"或"氧化物")。
(2)若A是能供给人类呼吸的气体,B是一种最常用的溶剂,D的水溶液显蓝色。则C—D反应的基本类型是____________;D—E反应的化学方程式是__________________________________________。
13.图KZ3-8中A~I是初中化学常见的物质,且分别是由H、C、O、Na、Al、S、Ca、Cu、Ag中的一种或几种元素组成的。在通常情况下,D与其他物质的状态不同,D、G、H、I均为单质,其中G为紫红色固体,H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能;B可用来改良酸性土壤;A、F均为由三种元素组成的盐。图中"—"表示两端的物质间能发生化学反应,"→"表示物质间存在转化关系,部分反应物、生成物或反应条件已略去。
(1)写出化学式:G________。
(2)写出A与C反应的化学方程式:________________________;
写出D与E反应的化学方程式:______________________________;
写出H→I反应的化学方程式:________________________________。
14.有A、B、C、D、E、F、G七种不同化合物,它们有如图KZ3-9所示的反应关系(图中的"—"表示相连两物质之间可以发生反应,图中的"→"表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物己略去)。若A能与B、D、F分别反应,C、G、E能顺时针转化,B、F、D又分别能转化生成C、G、E。已知:B和D;C和E;F和G分别为相同类型的物质,A是胃酸的主要成分,F为红色固体。请据图回答问题。
(1)F的化学式为________。
(2)写出C→G的化学反应方程式:_______________________________________。
15.现有一包固体粉末,可能含有FeCl3、Na2SO4、NaOH、CaCO3、NH4HCO3、Na2CO3中的一种或几种。现做如下实验:
(1)取少量固体加热,无氨味,则原固体中一定不含______________________。
(2)另取少量固体溶于水,得到无色澄清溶液,则原固体中一定不含________________。
(3)取(2)中溶液适量,滴加过量BaCl2溶液,出现白色沉淀,过滤得固体A和滤液B。固体A能全部溶于稀硝酸并产生气泡。则原固体中一定含有________,一定不含有________。
(4)向滤液B中通入CO2,产生白色沉淀,由此判断原固体中还含有NaOH。生成白色沉淀总反应的化学方程式为_______________________________________________________
参考答案
1.B
2.B [解析] 根据"一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种",结合框图,推测铜离子在溶液中显蓝色,NaOH和CuCl2会生成氢氧化铜沉淀,而氢氧化铜沉淀与稀硝酸反应生成硝酸铜;CaCO3和硝酸反应会生成气体,则蓝色溶液B中有硝酸铜、硝酸钙、稀硝酸,而原固体粉末一定有CaCO3、NaOH、CuCl2和Ca(NO3)2,无法确定是否含有NaCl、NaNO3。
3.B 4.C
5.(1)H2 H2O (2)2Cu+O2eq o(=====,s\up7(△))2CuO
(3)CuCl2+2NaOH===Cu(OH)2↓+2NaCl
[解析] (1)各物质均是初中化学常见物质,其中甲、乙、丙属于单质,A为黑色固体,C属于盐,C和E反应会生成氢氧化铜沉淀和氯化钠,所以C是氯化铜,E是氢氧化钠,A和D反应会生成氯化铜和B,所以A是氧化铜,D是盐酸,B就是水;甲+乙eq o(――→,s\up7(点燃))B,甲+丙eq o(――→,s\up7(△))A,所以甲是氧气,丙是铜,乙是氢气,经过验证,推导正确。
6.(1)Na2CO3
(2)H2SO4+BaCl2===BaSO4↓+2HCl
(3)2HCl+Na2CO3===2NaCl+H2O+CO2↑
7.(1)Ca(OH)2 化合反应 (2)纯碱(或苏打)
2NaOH+CO2===Na2CO3+H2O
[解析] A~G表示初中化学常见的物质,C是大理石的主要成分,所以C是碳酸钙,碳酸钙高温生成氧化钙和二氧化碳,所以E、F是氧化钙和二氧化碳,A、B生成的D会与F反应生成G和A,所以D是氢氧化钠,F是二氧化碳,氢氧化钠与二氧化碳反应生成碳酸钠和水,所以A是碳酸钠,G是水,E是氧化钙,所以B是氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,经过验证,推导正确,所以B的化学式为Ca(OH)2,反应④是氧化钙和水反应生成氢氧化钙,所以属于化学基本反应类型中的化合反应。
8.(1)Fe2O3 CuSO4
(2)Fe+CuSO4===Cu+FeSO4
(3)①③ (4)Fe2O3+6HCl===2FeCl3+3H2O
9.(1)Cu(OH)2 CO2
(2)复分解反应
(3)Cu+2AgNO3===2Ag+Cu(NO3)2
(4)燃料(或冶炼金属)
[解析] (1)A~K为中学常见的物质,H是一种建筑材料的主要成分,所以H是碳酸钙;气体F和溶液G反应会生成碳酸钙,所以F是二氧化碳,G是氢氧化钙;固体I和硝酸银反应会生成蓝色溶液J和银白色固体K,所以I是铜,J是硝酸铜,K是银;A为黑色粉末,A和气体E加热会生成铜和二氧化碳,所以A是氧化铜,E是一氧化碳;氧化铜会与溶液B反应,所以B是酸溶液,D是蓝色沉淀,所以D是氢氧化铜,经过验证,推导正确。
10.(1)CaO Na2CO3
(2)碳酸钙 CaCO3eq o(=====,s\up7(高温))CaO+CO2↑
(3)CO2+Ceq o(=====,s\up7(高温))2CO
2NaOH+Cu(NO3)2===Cu(OH)2↓+2NaNO3
(4)置换 (5)改良酸性土壤
[解析] 贝壳的成分是碳酸钙,高温煅烧生成氧化钙和二氧化碳,A是氧化物,可作干燥剂,所以A是氧化钙,B是二氧化碳,再根据框图可知,C就是氢氧化钙,又D是一种盐,用于制造玻璃,洗涤剂等,故D是碳酸钠,E为氢氧化钠,二氧化碳在高温下与碳反应生成一氧化碳,故F为一氧化碳,则G为铜,H为硝酸铜。
11.(1)O2 CaCO3
(2)C+CO2eq o(=====,s\up7(高温))2CO
(3)2CO2+2Na2O2===2Na2CO3+O2
[解析] D是大理石的主要成分,说明D是碳酸钙,这四种物质中均含有同一种元素,且B、C是氧化物,其中A是无色气体单质,A是氧气,B是有毒气体,B是一氧化碳,C是二氧化碳。
12.(1)CO2 酸
(2)置换反应 CuSO4+Ca(OH)2===Cu(OH)2↓+CaSO4(其他合理答案也可)
[解析] 根据A、B、C、D、E为初中化学常见的五种物质,若E为大理石的主要成分,则E是碳酸钙,A、B为组成元素相同的气体,所以B是二氧化碳,A是一氧化碳,D会与碳酸钙反应,所以D是酸,C会与一氧化碳、酸反应,所以C是金属氧化物;若A是能供给人类呼吸的气体,所以A是氧气,A、B会相互转化,B是一种最常用的溶剂,所以B是水,D的水溶液是蓝色,所以D可以是硫酸铜,B生成的E会与硫酸铜反应,所以E是氢氧化钙,C会与氧气、硫酸铜反应,所以C是铁,代入检验,符合题意。
13.(1)Cu
(2)Na2CO3+H2SO4===Na2SO4+H2O+CO2↑ CuO+H2eq o(=====,s\up7(△))Cu+H2O
Al+3AgNO3===Al(NO3)3+3Ag
[解析] 根据"H在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能",则推测H为铝;根据"G为紫红色固体",则推测G为铜;根据"B可用来改良酸性土壤",则推测B为氢氧化钙;根据"A、F均为由三种元素组成的盐",结合框图,则推测A、F分别为碳酸钠、硫酸铜;根据"在通常情况下,D与其他物质的状态不同,D、G、H、I均为单质""图中A~I是初中化学常见的物质,且分别是由H、C、O、Na、Al、S、Ca、Cu、Ag中的一种或几种元素组成的",则推测C可能为稀硫酸、D为氢气、E为氧化铜、I为银,代入检验,符合题意。
14.(1)Fe2O3
(2)CaCO3+2HCl===CaCl2+H2O+CO2↑
(或 CaCO3eq o(=====,s\up7(高温))CaO+CO2↑)
15.(1)NH4HCO3 (2)FeCl3、CaCO3
(3)Na2CO3 Na2SO4
(4)BaCl2+2NaOH+CO2===BaCO3↓+2NaCl+H2O

 加载中,请稍侯......
加载中,请稍侯......
精彩评论