一.选择题(共20小题)
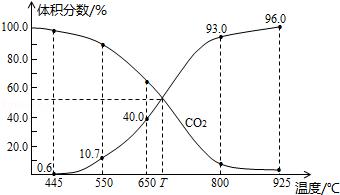
1.(2015•四川)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)⇌2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:已知气体分压(P分)=气体总压(P总)×体积分数,下列说法正确的是( )
A. 550℃时,若充入惰性气体,v正,v退均减小,平衡不移动
B. 650℃时,反应达平衡后CO2的转化率为25.0%
C. T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D. 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0P总
考点:化学平衡建立的过程;化学平衡的影响因素.
分析:A、可变的恒压密闭容器中反应,550℃时若充入惰性气体,相当于减小压强,则v正,v退均减小,又改反应是气体体积增大的反应,则平衡正向移动;
B、由图可知,650℃时,反应达平衡后CO的体积分数为40%,设开始加入的二氧化碳为1mol,根据三段式进行计算;
C、T℃时,反应达平衡后CO和CO2的体积分数都为50%,所以K=1,根据Qc与K的关系判断平衡移动方向;
D、925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=
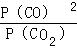
,据此计算;
解答:解:A、可变的恒压密闭容器中反应,550℃时若充入惰性气体,相当于减小压强,则v正,v退均减小,又改反应是气体体积增大的反应,则平衡正向移动,故A错误;
B、由图可知,650℃时,反应达平衡后CO的体积分数为40%,设开始加入的二氧化碳为1mol,转化了xmol,
则有C(s)+CO2(g)⇌2CO(g)
开始 1 0
转化 x 2x
平衡; 1﹣x 2x
所以
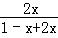
×100%=40%,解得x=0.25mol,则CO2的转化率为
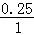
×100%=25%,故B正确;
C、T℃时,反应达平衡后CO和CO2的体积分数都为50%,所以Kp=
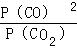
=1,则T℃时,若充入等体积的CO2和CO,Qc=1=K,所以平衡不移动,故C错误;
D、925℃时,CO的体积分数为96%,则CO2的体积分数都为4%,所以用平衡分压代替平衡浓度表示的化学平衡常数Kp=
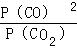
=

=23.0P,故D错误;
故选:B.
点评:本题考查了化学平衡图象、阅读题目获取信息的能力等,难度中等,需要学生具备运用信息与基础知识分析问题、解决问题的能力.
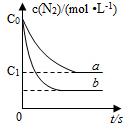
2.(2015•安徽)汽车尾气中NO产生的反应为:N2(g)+O2(g)⇌2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )
A. 温度T下,该反应的平衡常数K=
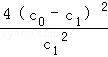
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
考点:化学平衡建立的过程;真题集萃.
分析:A、依据氮气的浓度变化,找出三段式,计算平衡常数即可;
B、此容器为恒容密闭容器,ρ=
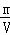
,据此判断即可;
C、催化剂只能改变化学反应色速率,不能改变物质的转化律;
D、由图可知,b曲线化学反应速率快,若是升高温度,氮气的平衡浓度减小,则正反应为吸热反应.
解答:解:A、N2(g)+O2(g)⇌2NO(g),
起(mol/L) c0c0 0
转(mol/L) x x 2x
平(mol/L) c1 c1 2x
解2x=2(c0 ﹣c1 ),故K=
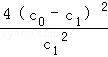
,故A正确;
B、反应物和生成物均是气体,故气体的质量m不变,容器为恒容容器,故V不变,那么密度ρ=
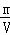
不变,故B错误;
C、由图可知,b曲线氮气的平衡浓度减小,故应是平衡发生移动,催化剂只能改变速率,不能改变平衡,故b曲线不可能是由于催化剂影响的,故C错误;
D、由图可知,b曲线化学反应速率快(变化幅度大),氮气的平衡浓度减小,升高温度平衡正向移动,则正反应为吸热反应,即△H>0,故D错误,故选A.
点评:本题主要考查的是化学平衡建立的过程,涉及平衡常数的计算、平衡移动原理的应用、催化剂对平衡的影响等,综合性较强,有一定难度.
3.(2015•上海)对于合成氨反应,达到平衡后,以下分析正确的是( )
A. 升高温度,对正反应的反应速率影响更大
B. 增大压强,对正反应的反应速率影响更大
C. 减小反应物浓度,对逆反应的反应速率影响更大
D. 加入催化剂,对逆反应的反应速率影响更大
考点:合成氨条件的选择.
分析:A、合成氨是发热反应,升温平衡逆向进行;
B、反应是气体体积减小的反应,增大压强平衡正向进行;
C、减小反应物浓度,平衡逆向进行;
D、催化剂同等程度影响正逆反应速.
解答:解:合成氨的化学方程式为:N2+3H2

2NH3,△H<0,反应是气体体积减小的发热反应,
A、合成氨是放热反应,升温平衡逆向进行,对逆反应的反应速率影响更大,故A错误;
B、反应是气体体积减小的反应,增大压强平衡正向进行,对正反应的反应速率影响更大,故B正确;
C、减小反应物浓度,平衡逆向进行,正反应减小的多,对正反应的反应速率影响更大,故C错误;
D、催化剂改变反应速率,不改变化学平衡,同等程度影响正逆反应速率,故D错误;
故选B.
点评:本题考查了化学平衡的影响因素分析判断,主要是费用特征和平衡移动原理的理解应用,掌握基础是关键,题目较简单.
4.(2014•天津)运用相关化学知识进行判断,下列结论错误的是( )
A. 某吸热反应能自发进行,因此该反应是熵增反应
B. NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
C. 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
D. 增大反应物浓度可加快反应速度,因此用浓硫酸与铁反应能增大生成H2的速率
考点:焓变和熵变;使用化石燃料的利弊及新能源的开发;化学反应速率的影响因素;硅和二氧化硅.
专题:化学反应中的能量变化;化学反应速率专题.
分析:A、吸热反应可以自发进行,必须是熵增的反应,依据反应自发进行的判断是△H﹣T△S<0分析;
B、氟化铵水解生成氟化氢,氢氟酸腐蚀玻璃;
C、海底由天然气与水在高压低温条件下形成的类冰状的结晶物质;
D、常温下铁在浓硫酸中钝化.
解答:解:A、吸热反应可以自发进行,△H>0,若满足△H﹣T△S<0,必须是熵增的反应,故A正确;
B、氟化铵水解生成氟化氢,氢氟酸和玻璃中二氧化硅反应腐蚀玻璃,因此NH4F溶液不能存放于玻璃试剂瓶中,故B正确;
C、海底中天然气与水在高压低温条件下形成的类冰状的结晶物质,为可燃冰,故C正确;
D、常温下铁在浓硫酸中钝化,表面形成致密氧化物薄膜阻止浓硫酸与铁反应,不能生成氢气,故D错误;
故选D.
点评:本题考查了物质性质,盐类水解分析应用,注意常温铁在浓硫酸中发生钝化现象,题目较简单.
5.(2014春•天津期末)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
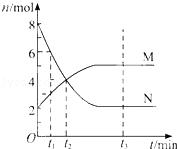
A. 反应的化学方程式为:2M⇌N
B. t2时,正逆反应速率相等,达到平衡
C. t3时,正反应速率大于逆反应速率
D. t1时,N的浓度是M浓度的2倍
考点:化学反应速率变化曲线及其应用;物质的量或浓度随时间的变化曲线.
专题:图示题;化学平衡专题.
分析:A、根据图象判断出反应物和生成物,根据物质的量的变化判断计量数之间的关系;
B、根据某一时间反应中各物质的物质的量是否变化判断反应是否达到平衡;
C、根据平衡移动的方向判断正逆反应速率的关系;
D、根据某一时刻反应物和生成物的物质的量多少判断浓度的关系.
解答:解:A、由图象可知,反应中M的物质的量逐渐增多,N的物质的量逐渐减少,则在反应中N为反应物,M为生成物,图象中,在相等的时间内消耗的N和M的物质的之比为2:1,所以反应方程式应为:2N

M,故A错误;
B、由图可知t2时,反应没有达到平衡,此时反应继续向正方向移动,正反应速率大于逆反应速率,故B错误;
C、由图可知t3时,反应达到平衡,正逆反应速率相等,故C错误;
D、t1时,N的物质的量为6mol.M的物质的量为3mol,故N的浓度是M浓度的2倍,故D正确.
故选D.
点评:本题考查化学反应速率与化学平衡知识,做题时注意从反应物和生成物的物质的量的变化角度,判断反应物和生成物以及反应是否达到平衡,题目难度一般.
6.(2014•重庆)在恒容密闭容器中通入X并发生反应:2X(g)⇌Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示.下列叙述正确的是( )
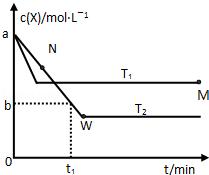
A. 该反应进行到M点放出的热量大于进行到W点放出的热量
B. T2下,在0~t1时间内,v(Y)=
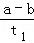
mol•L﹣1•min﹣1
C. M点的正反应速率V正大于N点的逆反应速率V逆
D. M点时再加入一定量X,平衡后X的转化率减小
考点:体积百分含量随温度、压强变化曲线.
专题:化学平衡专题.
分析:由图可知,温度为T1先到达平衡,所以T1>T2,温度越高,平衡时X的物质的量浓度越大,说明升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故逆反应为吸热反应,正反应为放热反应;
A、根据图象判断参加反应的X的量的多少,反应的X越多,放热越多;
B、根据图中X的浓度变化求出Y的浓度变化,再求反应速率;
C、温度越高反应速率越大;
D、M点时再加入一定量X,达到的新平衡与原平衡比较,根据压强对平衡的影响分析.
解答:解:由图可知,温度为T1先到达平衡,所以T1>T2,温度越高,平衡时X的物质的量浓度越大,说明升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故逆反应为吸热反应,正反应为放热反应;
A、进行到M点X的转化率较低,由于正向是放热反应,所以反应进行到M点放出的热量少,故A错误;
B、T2下,在0~t1时间内,X的浓度变化为:c(X)=(a﹣b)mol/L,则Y的浓度变化为c(Y)=
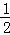
c(X)=
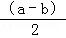
mol/L,所以v(Y)=
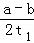
mol•L﹣1•min﹣1,故B错误;
C、根据图象可知,温度为T1时反应首先达到平衡状态;温度高反应速率快,到达平衡的时间少,则温度是T1>T2;M点温度高于N点温度,且N点反应没有达到平衡状态,此时反应向正反应方向进行,即N点的逆反应速率小于N点的正反应速率,因此M点的正反应速率大于N点的逆反应速率,故C正确;
D、M点时再加入一定量X,达到的新平衡与原平衡比较,压强增大,增大压强平衡正移,则X的转化率增大,所以M点时再加入一定量X,平衡后X的转化率增大,故D错误;
故选C.
点评:本题考查了化学平衡图象问题、平衡有关计算、外界条件对平衡移动影响等,难度中等,根据图象判断反应为放热反应是解题的关键.注意把握图象中曲线的变化特点,分析外界条件对化学平衡的影响.
7.(2013•江苏)下列有关说法正确的是( )
A. 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B. 电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C. CH3COOH 溶液加水稀释后,溶液中
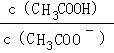
的值减小
D. Na2CO3溶液中加入少量Ca(OH)2 固体,CO32﹣水解程度减小,溶液的pH 减小
考点:焓变和熵变;铜的电解精炼;弱电解质在水溶液中的电离平衡;影响盐类水解程度的主要因素.
专题:化学平衡专题;电离平衡与溶液的pH专题;电化学专题.
分析:A、根据本反应前后气体变固体,熵变小于零,只有在焓变小于零时自发;
B、用电解法精炼精铜时,粗铜作阳极,纯铜作阴极;
C、根据CH3COOH溶液加水稀释,平衡向正反应方向移动,n(CH3COOH)减小,n(CH3COO﹣)增大,以及
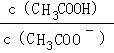
=
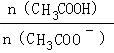
来分析;
D、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32﹣水解程度减小,但两者反应生成了NaOH,溶液的pH增大.
解答:解:A、本反应前后气体变固体,熵变小于零,只有在焓变小于零时自发,即该反应的△H<0,故A正确;
B、用电解法精炼精铜时,粗铜作阳极,纯铜作阴极,故B错误;
C、根据CH3COOH溶液加水稀释,平衡向正反应方向移动,n(CH3COOH)减小,n(CH3COO﹣)增大,
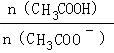
减小,所以
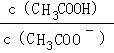
减小,故C正确;
D、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32﹣水解程度减小,但两者反应生成了NaOH,溶液的pH增大,故D错误;
故选AC.
点评:本题是化学反应与热效应、电化学等的简单综合题,着力考查学生对用熵变焓变判断反应方向,水解反应、电解池等方面的能力.
8.(2013•福建)NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L﹣1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
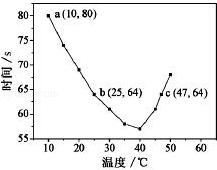
A. 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B. 图中b、c两点对应的NaHSO3反应速率相等
C. 图中a点对应的NaHSO3反应速率为5.0×10﹣5mol•L﹣1•s﹣1
D. 温度高于40℃时,淀粉不宜用作该实验的指示剂
考点:化学反应速率的影响因素.
专题:压轴题;化学反应速率专题.
分析:A.由图可知,40℃之前,温度高反应速率加快,40℃之后温度高,变色时间越长;
B.b、c点对应的温度不同;
C.a点时间为80s,浓度变化量为
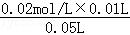
=0.004mol/L;
D.结合55℃时,没有出现蓝色分析.
解答:解:A.从图象中可以看出,40℃以前,温度越高,反应速度越快,40℃后温度越高,变色时间越长,反应越慢,而55℃,未变蓝,淀粉发生了水解,故A正确;
B.由图中b、c反应时间相同、温度不同可知,温度高反应速率快,故反应速率不同,故B错误;
C.a点时间为80s,浓度变化量为
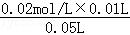
=0.004mol/L,a点对应的NaHSO3反应速率为5.0×10﹣5mol•L﹣1•s﹣1,故C正确;
D.55℃时,没有出现蓝色,淀粉发生水解反应,故淀粉已不能作为该反应的指示剂,故D正确;
故选B.
点评:本题考查化学反应速率的影响因素,侧重图象分析及温度对反应的影响,注意不同温度下均可被过量KIO3氧化,注重分析能力和解决问题能力的考查,题目难度较大.
9.(2013•江苏)一定条件下存在反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol CO和1mol H2O,在Ⅱ中充入1mol CO2 和1mol H2,在Ⅲ中充入2mol CO 和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是( )
A. 容器Ⅰ、Ⅱ中正反应速率相同
B. 容器Ⅰ、Ⅲ中反应的平衡常数相同
C. 容器Ⅰ中CO 的物质的量比容器Ⅱ中的多
D. 容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和小于1
考点:化学平衡的影响因素.
专题:压轴题;化学平衡专题.
分析:A.容器Ⅰ中从正反应开始到达平衡,容器Ⅱ中从逆反应开始到达,平衡建立的途径不相同;
B.容器Ⅲ中相当于在容器Ⅰ中平衡的基础上再加入1mol CO和1mol H2O,反应向正反应进行,故容器Ⅲ中到达平衡时温度更高,该反应正反应是放热反应,温度越高平衡常数越小;
C.容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动;
D.温度相同时,容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1,容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动.
解答:解:A.容器Ⅰ中从正反应开始到达平衡,容器Ⅱ中从逆反应开始到达,平衡建立的途径不相同,无法比较反应速率,故A错误
B.容器Ⅲ中相当于在容器Ⅰ中平衡的基础上再加入1mol CO和1mol H2O,反应向正反应进行,故容器Ⅲ中到达平衡时温度更高,该反应正反应是放热反应,温度越高平衡常数越小,故B错误;
C.容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动,故容器Ⅰ中CO 的物质的量比容器Ⅱ中的多,故C正确;
D.温度相同时,容器I中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1,容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动,二氧化碳的转化率比两容器相同温度时容器Ⅱ中CO2的转化率低,故容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和小于1,故D正确;
故选CD.
点评:本题考查影响化学平衡的因素、化学平衡的建立等,难度较大,构建平衡建立的途径进行比较是关键.
10.(2013•上海)某恒温密闭容器中,可逆反应A(s)⇌B+C(g)﹣Q达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
A. 产物B的状态只能为固态或液态
B. 平衡时,单位时间内n(A)消耗:n(C)消耗=1:1
C. 保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D. 若开始时向容器中加入1mol B和1mol C,达到平衡时放出热量Q
考点:化学平衡的计算;化学平衡的影响因素.
专题:化学平衡专题.
分析:A、若B为气体,因容器保持恒温,缩小容器体积,达到新平衡时平衡常数不变,则气体C的浓度也一定不变;
B、平衡时,各物质的量不再改变,正反应速率和逆反应速率相等,因此单位时间内n(A)消耗=n(C)消耗;
C、保持体积不变,若B为气态,则向平衡体系中加入B,平衡逆向移动;
D、因反应为可逆反应,故加入1molB和1molC至反应达到平衡时不能完全消耗,放出热量小于Q;
解答:解:A、若B是气体,平衡常数K=c(B)•c(C),若B是非气体,平衡常数K=c(C),由于C(g)的浓度不变,因此B可以是气体或是非气体,A项错误;
B、平衡时,各物质的量不再改变,正反应速率和逆反应速率相等,因此单位时间内n(A)消耗=n(C)消耗,故B项正确;
C、保持体积不变,B可以是气体或是非气体,则向平衡体系中加入B,平衡可能不移动,C项正确;
D、因反应为可逆反应,故加入1molB和1molC至反应达到平衡时转化率一定小于100%,因此放出热量小于Q,故D项错误;
故选BC.
点评:本题考查化学平衡影响因素的分析判断,化学判断移动原理的理解设计解题关键,题目难度中等.
11.(2012•福建)一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
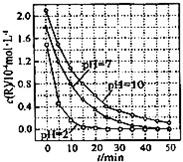
A. 在0﹣50min之间,pH=2和pH=7 时R的降解百分率相等
B. 溶液酸性越强,R 的降解速率越小
C. R的起始浓度越小,降解速率越大
D. 在 20﹣25min之间,pH=10 时 R 的平均降解速率为 0.04mol•L﹣1•min﹣1
考点:化学反应速率的影响因素;反应速率的定量表示方法.
专题:压轴题;化学反应速率专题.
分析:A、根据图中的信息可以知道在0﹣50min之间,pH=2和pH=7时R的降解百分率;
B、对比溶液的酸性强弱对R的降解速率的影响情况;
C、可以根据同一pH条件下,图示R的起始浓度与降解速率的关系来判断;
D、根据平均降解速率v=
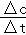
来计算即可.
解答:解:A、根据图示可知:在0﹣50min之间,pH=2和pH=7时R的降解百分率都为100%,故A正确;
B、溶液酸性越强,即pH越小,线的斜率越大,可以知道R的降解速率越大,故B错误;
C、同一pH条件下,R的起始浓度与降解速率的关系:曲线斜率增大,则降解速率越小,即R的起始浓度越小,降解速率越小,故C错误;
D、在 20﹣25min之间,pH=10时R的平均降解速率为
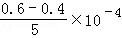
=0.04×10﹣4mol•L﹣1•min﹣1,故D错误.
故选A.
点评:本题考查学生的识图能力,要求学生具有分析和解决问题的能力,难度不大.
12.(2012•海南)下列实验操作正确的是( )
A. 可用氨水除去试管内壁上的银镜
B. 硅酸钠溶液应保存在带玻璃塞的试剂瓶中
C. 将三氯化铁溶液蒸干,可制得无水三氯化铁
D. 锌与稀硫酸反应时,要加大反应速率可滴加少量硫酸铜
考点:化学反应速率的影响因素;盐类水解的应用;硅和二氧化硅.
专题:实验评价题.
分析:A、银与氨水不反应;
B、硅酸钠是无机矿物胶,具有粘合性,使瓶塞与试剂瓶粘在一起;
C、氯化铁溶液中存在平衡Fe3++3H2O⇌Fe(OH)3+3HCl,加热HCl挥发,促进水解彻底进行;
D、滴加少量CuSO4溶液,Zn置换出Cu,构成原电池.
解答:解:A、银与氨水不反应,不能除去试管内壁上的银镜,故A错误;
B、硅酸钠是无机矿物胶,具有粘合性,使瓶塞与试剂瓶粘在一起,应使用橡胶塞,故B错误;
C、氯化铁溶液中存在平衡Fe3++3H2O⇌Fe(OH)3+3HCl,加热HCl挥发,促进水解彻底进行,将三氯化铁溶液蒸干,可制得Fe(OH)3,不能获得无水三氯化铁,故C错误;
D、滴加少量CuSO4溶液,Zn置换出Cu,构成原电池,加快反应速率,故D正确;
故选D.
点评:本题考查盐类水解、影响反应速率的盐酸、元素化合物性质等,难度中等,注意C中盐类水解彻底进行的原因.
13.(2012•重庆)在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g)⇌2c(g);△H1<0
x(g)+3y(g)⇌2z(g);△H2>0
进行相关操作且达到平衡后(忽略体积改变所作的功),下列叙述错误的是( )
A. 等压时,通入惰性气体,c的物质的量不变
B. 等压时,通入z气体,反应器中温度升高
C. 等容时,通入惰性气体,各反应速率不变
D. 等容时,通入z气体,y的物质的量浓度增大
考点:化学平衡的影响因素.
专题:压轴题;化学平衡专题.
分析:A、等压时,通入惰性气体,体积增大,对第二个反应平衡向逆反应移动,温度升高,导致第一个反应向逆反应移动;
B、等压时,通入z气体,第二反应平衡向逆反应移动,反应器中温度升高;
C、等容时,通入惰性气体,各反应混合物的浓度不变;
D、等容时,通入z气体,第二反应平衡向逆反应移动.
解答:解:A、等压时,通入惰性气体,容器体积增大,等效为压强减小,平衡x(g)+3y(g)⇌2z(g)(△H>0)向左移动,正反应为放热反应,反应体系的温度降低,由于该反应容器是一个不导热的容器,所以平衡a(g)+b(g)⇌2c(g)也向由(吸热方向)移动,c的物质的量增大,故A错误;
B、等压时,通入z气体,增大了生成物的浓度,平衡x(g)+3y(g)⇌2z(g)向左移动,由于该反应的逆反应是放热反应,容器内温度升高,虽然导致第一个反应向逆反应移动,但移动结果不会恢复到原温度,故平衡时温度升高,故B正确;
C、等容时,通入惰性气体,各反应物和生成物的物质的量没有变化,即各组分的浓度没有发生变化,所以各组分的反应速率不发生变化,故C正确;
D、等容时,通入z气体,增大了生成物z的浓度,平衡逆向移动,所以y的物质的量浓度增大,故D正确;
故选A.
点评:本题考查外界条件对化学平衡的影响,难度中等,本题要特别注意题干中的信息"不导热的密闭反应器",注意压强对第一个反应没有影响,根据第二反应的移动热效应,判断第一个反应的移动.
14.(2012•天津)已知2SO2 (g)+O2 (g)⇌2SO3 (g);△H=﹣197kJ•mol﹣1.向同温、同体积的三个密闭容器中分别充入气体:(甲) 2mol SO2和1mol O2;(乙) 1mol SO2和0.5mol O2;(丙) 2mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是( )
A. 容器内压强P:P甲=P丙>2P乙
B. SO3的质量m:m甲=m丙>2m乙
C. c(SO2)与c(O2)之比k:k甲=k丙>k乙
D. 反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
考点:等效平衡.
专题:压轴题;化学平衡专题.
分析:恒温恒容,甲与乙起始n(SO2):n(O2)=2:1,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,故甲中转化率增大;丙按化学计量数转化到左边可得n(SO2)=2mol,n(O2)=1mol,与甲为等效平衡,平衡时对应各组分的物质的量相等,据此结合选项解答;
解答:解:恒温恒容,甲与乙起始n(SO2):n(O2)=2:1,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,转化率增大;丙按化学计量数转化到左边可得n(SO2)=2mol,n(O2)=1mol,与甲为等效平衡,平衡时对应个组分的物质的量相等,
A、甲与丙为等效平衡,平衡时对应各组分的物质的量相等,故压强P甲=P丙,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,故P乙<P甲<2P乙,故P甲=P丙<2P乙,故A错误;
B、甲与丙为等效平衡,平衡时对应各组分的物质的量相等,故质量m甲=m丙,甲等效为在乙到达平衡的基础上,再加入1mol SO2和0.5mol O2,增大压强,平衡向正反应移动,SO2转化率增大,m甲>2m乙,故m甲=m丙>2m乙,故B正确;
C、对于甲、乙,SO2、O2起始物质的量之比等于化学计量数之比,c(SO2)与c(O2)之比为定值2:1,丙为分解反应,丙中c(SO2)与c(O2)之比为2:1,故k甲=k丙=k乙=2,故C错误;
D、甲与丙为等效平衡,平衡时对应各组分的物质的量相等,故Q甲+Q丙=197,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,SO2转化率增大,故Q甲>2Q乙,故D错误;
故选B.
点评:该题考查化学平衡移动与计算、反应热知识、等效平衡等,难度较大,注意构建甲、乙平衡建立的途径,注意理解等效平衡.
15.(2011•海南)对于可逆反应H2(g)+I2(g)⇌2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
A. H2(g)的消耗速率与HI(g)的生成速率之比为2:1
B. 反应进行的净速率是正、逆反应速率之差
C. 正、逆反应速率的比值是恒定的
D. 达到平衡时,正、逆反应速率相等
考点:化学平衡状态的判断;反应速率的定量表示方法.
专题:化学平衡专题.
分析:A.反应速率之比等于化学计量数之比;
B.可逆反应正逆反应同时进行,净速率是正、逆反应速率之差;
C.反应状态不同,正逆反应速率关系不确定;
D.当正逆反应速率相等时达到平衡状态.
解答:解:A.由反应可知,H2(g)的消耗速率与HI(g)的生成速率之比为1:2,故A错误;
B.可逆反应正逆反应同时进行,净速率是正、逆反应速率之差,故B正确;
C.反应状态不同,正逆反应速率关系不同,二者只要不达到平衡状态,则没有恒定的关系,故C错误;
D.当正逆反应速率相等时,化学反应达到平衡状态,故D正确.
故选BD.
点评:本题考查化学平衡问题,题目难度不大,易错点为B,注意反应的净速率与正逆反应速率的关系.
16.(2011•天津)向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)⇌SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右所示.由图可得出的正确结论是( )
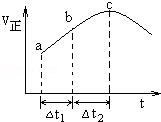
A. 反应在c点达到平衡状态
B. 反应物浓度:a点小于b点
C. 反应物的总能量低于生成物的总能量
D. △t1=△t2时,SO2的转化率:a~b段小于b~c段
考点:化学反应速率变化曲线及其应用;化学平衡建立的过程.
专题:压轴题.
分析:由题意可知一个反应前后体积不变的可逆反应,由于容器恒容,因此压强不影响反应速率,所以在本题中只考虑温度和浓度的影响.结合图象可知反应速率先增大再减小,因为只要开始反应,反应物浓度就要降低,反应速率应该降低,但此时正反应却是升高的,这说明此时温度的影响是主要的,由于容器是绝热的,因此只能是放热反应,从而导致容器内温度升高反应速率加快.
解答:解:A、化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,c点对应的正反应速率显然还在改变,故一定未达平衡,故A错误;
B、a到b时正反应速率增加,反应物浓度随时间不断减小,故B错误;
C、从a到c正反应速率增大,之后正反应速率减小,说明反应刚开始时温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,说明该反应为放热反应,即反应物的总能量高于生成物的总能量,故C错误;
D、随着反应的进行,正反应速率越快,消耗的二氧化硫就越多,则SO2的转化率将逐渐增大,故D正确;
故选:D.
点评:本题难就难在没有直接告诉同学们横坐标表示什么.结合图象分析题意就很关键了.
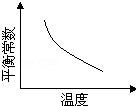
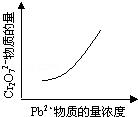
17.(2011•安徽)电镀废液中Cr2O72﹣可通过下列反应转化成铬黄(PbCrO4):Cr2O72﹣(aq)+2Pb2+(aq)+H2O(l)⇌2PbCrO4(s)+2H+(aq)△H<0该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是( )
A.
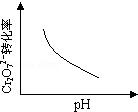
B.
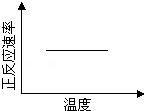
C.
D.
考点:物质的量或浓度随时间的变化曲线;化学平衡常数的含义;化学反应速率变化曲线及其应用;转化率随温度、压强的变化曲线.
专题:图示题;热点问题;化学平衡专题.
分析:根据图象中纵横坐标的意义,利用温度、浓度对化学反应速率及化学平衡的影响来分析一个量随另一个量的变化,变化趋势与图中符合的即为正确答案.
解答:解:A、由△H<0,则正反应是一个放热的反应,升高温度平衡向吸热的方向移动,即向逆反应方向移动,由平衡常数为生成物浓度幂之积与反应物浓度幂之积,则K减小,故A正确;
B、pH增大溶液,则碱性增强,会中和溶液中H+,降低生成物浓度,平衡向正方应方向移动,Cr2O72﹣的转化率会增大,与图中不符,故B错误;
C、温度升高,正、逆反应速率都增大,与图中不符,故C错误;
D、增大反应物Pb2+的浓度,平衡向正方应方向移动,则Cr2O72﹣的物质的量会减小,与图中不符,故D错误;
故选:A.
点评:本题考查影响化学平衡移动和化学反应速率的因素,注重了与图象相结合来考查学生,明确图象中纵横坐标表示的量,学生应学会将理论分析与图象有机的结合在一起即可解答,难度不是很大.
18.(2010•安徽)低脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
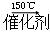
2N2(g)+3H2O(g)△H<0在恒容的密闭容器中,下列有关说法正确的是( )
A. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B. 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C. 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
考点:化学平衡的影响因素;化学平衡常数的含义;化学平衡状态的判断.
分析:A、从平衡移动的方向判断平衡常数的变化;
B、可逆反应中,加入一种反应物,平衡向正方向移动,以此判断转化率变化;
C、反应达到平衡时,正逆反应速率相等;
D、催化剂能加快反应速率,但不影响平衡的移动.
解答:解:A、放热反应升温,平衡向逆反应方向移动,平衡常数减小,故A错误;
B、增大一个反应物浓度另一反应物转化率增大,故B错误;
C、单位时间内消耗NO和N2的物质的量比为1:2时,正逆反应速率相等,故C正确.
D、使用催化剂平衡不移动,故D错误.
故选C.
点评:本题考查外界条件对化学反应速率的影响,平衡状态的判断等问题,做题时注意平衡常数的变化以及平衡状态的判断方法等问题.
19.(2010•重庆)当反应COCl2(g)⇌CO(g)+Cl2(g)△H>0 达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A. ①②④B. ①④⑥C. ②③⑥D. ③⑤⑥
考点:化学平衡的影响因素.
专题:化学平衡专题.
分析:化学反应COCl2(g)⇌CO(g)+Cl2(g)△H>0;是气体体积增大的反应,正向反应是吸热反应;转化率的变化根据化学平衡的移动方向分析判断
①升温平衡向吸热反应方向移动;
②恒容通入惰性气体,总压增大,分压不变,平衡不动;
③增加CO的浓度,平衡逆向进行;
④减压平衡向气体体积增大的方向进行,平衡正向进行;
⑤加催化剂,改变速率不改变平衡;
⑥恒压通入惰性气体,压强增大,为保持恒压,体积增大压强减小,平衡正向进行.
解答:解:化学反应COCl2(g)⇌CO(g)+Cl2(g)△H>0;是气体体积增大的反应,正向反应是吸热反应;转化率的变化根据化学平衡的移动方向分析判断
①升温平衡向吸热反应方向移动;平衡正向进行,COCl2转化率增大,故①符合;
②恒容通入惰性气体,总压增大,分压不变,平衡不动;COCl2转化率不变,故②不符合;
③增加CO的浓度,平衡逆向进行;COCl2转化率减小,故③不符合;
④减压平衡向气体体积增大的方向进行,平衡正向进行;COCl2转化率增大,故④符合;
⑤加催化剂,改变速率不改变平衡;COCl2转化率不变,故⑤不符合;
⑥恒压通入惰性气体,压强增大,为保持恒压,体积增大压强减小,平衡正向进行;COCl2转化率增大,故⑥符合;
综上所述:①④⑥正确,
故选B.
点评:本题考查了化学平衡的影响因素的分析判断,体积改变,平衡移动方向是判断的关键,题目难度中等.
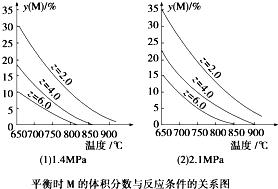
20.(2010•四川)反应aM(g)+bN(g)⇌cP(g)+dQ(g)达到平衡时.M的体积分数y(M)与反应条件的关系如图所示.其中Z表示反应开始时N的物质的量与M的物质的量之比.下列说法正确的是( )
A. 同温同压Z时,加入催化剂,平衡时Q的体积分数增加
B. 同压同Z时,升高温度,平衡时Q的体积分数增加
C. 同温同Z时,增加压强,平衡时Q的体积分数增加
D. 同温同压时,增加Z,平衡时Q的体积分数增加
考点:化学平衡的影响因素.
专题:压轴题;化学平衡专题.
分析:A、催化剂同程度影响化学反应速率,对平衡移动无影响;
B、对比(1)(2)两个图象,温度升高,M的体积分数减小,说明正反应为吸热反应;
C、同温同Z时,增加压强,M的体积分数增大,说明a+b<c+d,平衡向逆反应方向移动;
D、由图象可知,Z值越大,M的体积分数越小,有利于M的转化率的提高,但Q的体积分数不一定增大.
解答:解:A、催化剂同程度影响正、逆化学反应速率,对平衡移动无影响,同温同压同Z时,加入催化剂,平衡时Q的体积分数不变,故A错误;
B、对比(1)(2)两个图象,温度升高,M的体积分数减小,说明正反应为吸热反应,同压同Z时,升高温度,平衡向正反应方向移动,则平衡时Q的体积分数增加,故B正确
C、同温同Z时,增加压强,M的体积分数增大,说明a+b<c+d,平衡向逆反应方向移动,则Q的体积分数减小,故C错误;
D、由图象可知,Z值越大,M的体积分数越小,有利于M的转化率的提高,但Q的体积分数不一定增大,如加入N的物质的量较多,虽然有利于平衡右移,但Q的体积分数依然较小,故D错误;
故选B.
点评:本题考查化学平衡移动图象问题的分析,难度中等,注意对比两个图象曲线变化特征,分析温度、压强对平衡移动的影响.

 加载中,请稍侯......
加载中,请稍侯......
精彩评论